题目内容
【题目】某溶液由NaOH、HCl、H2SO4和MgCl2中的一种或几种组成。向该溶液中滴加Ba(OH)2 溶液,产生沉淀的质量与加入Ba(OH)2 溶液体积的关系如图所示。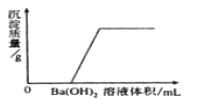
请你从图中获得的信息来分析,该溶液中不可能存在的物质是;写出产生沉淀的化学方程式是。
【答案】H2SO4和NaOH;MgCl2+ Ba(OH)2=Mg(OH)2↓+ BaCl2
【解析】硫酸根离子和钡离子只要接触就会生成硫酸钡沉淀,而沉淀的起点不是从零开始,所以一定没有硫酸,沉淀从x轴的某一点开始,说明了开始部分在发生中和反应,一定有盐酸和氯化镁,有盐酸和氯化镁就不含有氢氧化钠,则一定存在的是HCl、MgCl2 , 一定不存在的是NaOH、H2SO4 , 滴加氢氧化钡溶液生成的沉淀为氢氧化镁,发生反应的化学方程式为:MgCl2+ Ba(OH)2=Mg(OH)2↓+ BaCl2。
故答案为:(1)H2SO4和NaOH(2)MgCl2+ Ba(OH)2=Mg(OH)2↓+ BaCl2从图像上看刚加入氢氧化钡没有沉淀,可得出原混合液中有硫酸,同时可以获知原溶液显酸性,因此必含有盐酸,后又有沉淀,说明原溶液中有氯化铜,进而可以排除氢氧化钠

练习册系列答案
相关题目