题目内容
【题目】如图表示X、Y、Z三种物质的溶解度曲线,下列说法错误的是( )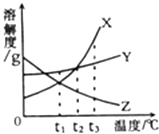
A.Y中含有少量X,用海水晒盐的原理提纯Y
B.t1℃时,三种物质的饱和溶液升温到t2℃,溶液中溶质质量分数的大小关系是Y>X>Z
C.t3℃时,X、Y的饱和溶液降温到t2℃,析出晶体较多的是X
D.t3℃时,等质量的X、Y分别配成该温度下的饱和溶液,所得溶液质量X<Y
【答案】C
【解析】A海水晒盐的原理是蒸发,Y的溶解度随温度的变化变化不大,采用蒸发结晶的方法提纯,A不符合题意;
B由溶解度曲线可知,X、y的溶解度随温度的升高而增大,故升温后溶质的质量分数不变,Z的溶解度随温度的升高而减小,故升温后有晶体析出,溶质的质量分数变小,B不符合题意;
C、t3℃时,等质量的X、Y的饱和溶液降温到t2℃,析出晶体较多的是X,C符合题意;
D、t3℃时时X的溶解度比Y的大,即等质量的X、Y溶解时Y需要的溶剂的量更多,配成该温度下的饱和溶液,所得溶液质量X<Y,D不符合题意。
故答案为:CA根据物质的溶解度随温度的变化情况可以得到提纯的方法
B根据三种物质的溶解度随温度的变化情况可解答
C根据不饱和溶液的质量关系可解答
D根据t3℃时两物质的溶解度来解答

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案
相关题目