题目内容
【题目】某化学探究活动小组欲用实验制得的一氧化碳(其中混有水蒸气和二氧化碳)来测定赤铁矿中氧化铁的含量,设计了如图所示的实验装置(其中无水硫酸铜遇水能由白色变为蓝色,碱石灰为氢氧化钠和氧化钙的混合物). 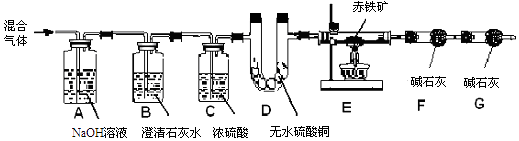
请按要求回答下列问题:
(1)D装置作用是证明进入E装置的气体中无水蒸气,则B装置的作用是;G装置的作用是 .
(2)E装置中发生反应的化学方程式为 , 小峰同学通过称量F装置反应前、后的质量来计算,若按这一方案进行实验,则还缺少的一个数据是 .
(3)如将A、B装置连接在D、E之间,并记录小峰同学所需的数据,则计算出氧化铁的含量(填“偏大”、“偏小”或“相同”).
(4)请你指出探究活动小组设计的这个实验方案的明显不足之处: .
【答案】
(1)检验二氧化碳是否完全除净;防止空气中的二氧化碳和水蒸气进入装置F造成误差
(2)Fe2O3+3CO ![]() 2Fe+3CO2;赤铁矿样品的质量
2Fe+3CO2;赤铁矿样品的质量
(3)偏大
(4)缺少尾气处理装置
【解析】解:(1)A中的氢氧化钠溶液可以除去混合气体中的二氧化碳,则装置B中的澄清的石灰水是用来检验二氧化碳是否完全除净;G中的碱石灰是为了防止空气中的二氧化碳和水蒸气进入装置F造成误差;故填:检验二氧化碳是否完全除净;防止空气中的二氧化碳和水蒸气进入装置F造成误差;(2)工业常用赤铁矿(主要成分为氧化铁)和一氧化碳在高温条件下炼铁,该反应的化学方程式为:Fe2O3+3CO ![]() 2Fe+3CO2;通过称量F装置反应前、后的质量差就是生成二氧化碳的质量,利用化学方程式,根据二氧化碳的质量计算出氧化铁的质量,要想计算出赤铁矿中氧化铁的含量还必须要知道赤铁矿样品的质量; 所以答案是:Fe2O3+3CO
2Fe+3CO2;通过称量F装置反应前、后的质量差就是生成二氧化碳的质量,利用化学方程式,根据二氧化碳的质量计算出氧化铁的质量,要想计算出赤铁矿中氧化铁的含量还必须要知道赤铁矿样品的质量; 所以答案是:Fe2O3+3CO ![]() 2Fe+3CO2;赤铁矿样品的质量;(3)如将A、B装置连接在D、E之间,就没有将气体中混有的水蒸气完全除去,造成装置F中增重的质量偏大,则计算出氧化铁的含量偏大;故填:偏大;(4)反应后的尾气中含有有毒的一氧化碳气体,不能直接排放到空气中,要进行尾气的处理,以防造成空气污染;故填:缺少尾气处理装置.
2Fe+3CO2;赤铁矿样品的质量;(3)如将A、B装置连接在D、E之间,就没有将气体中混有的水蒸气完全除去,造成装置F中增重的质量偏大,则计算出氧化铁的含量偏大;故填:偏大;(4)反应后的尾气中含有有毒的一氧化碳气体,不能直接排放到空气中,要进行尾气的处理,以防造成空气污染;故填:缺少尾气处理装置.
【考点精析】根据题目的已知条件,利用一氧化碳还原氧化铁和书写化学方程式、文字表达式、电离方程式的相关知识可以得到问题的答案,需要掌握原理:在高温下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石里还原出来;注意:a、配平 b、条件 c、箭号.