题目内容
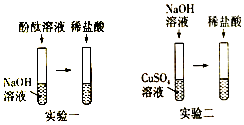
【题目】将某氢氧化钠溶液逐滴滴入硫酸和硫酸铜的混合溶液中,直至过量.根据实验事实绘制如图所示曲线.其中说法正确的是( ) 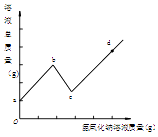
A.a至b段有蓝色沉淀生成
B.a至c段硫酸钠质量不断增大
C.c至d段,溶液pH不断减小
D.c点比a点所含的溶质种类多
【答案】B
【解析】解:A、a至b时,氢氧化钠和硫酸反应生成硫酸钠和水,蓝色没有沉淀生成,该选项说法不正确; B、a至b时,反应生成硫酸钠,b至c时,氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,因此a至c段硫酸钠质量不断增大,该选项说法正确;
C、c至d段是硫酸和硫酸铜完全反应后继续加入氢氧化钠溶液,溶液的碱性增强,pH不断升高,该选项说法不正确;
D、a点时溶液中的溶质是硫酸和硫酸铜,c点时溶液中的溶质是硫酸钠,因此c点比a点所含的溶质种类少,该选项说法不正确.
故选:B.

 阅读快车系列答案
阅读快车系列答案【题目】有关物质组成及化学规律的发现对化学的发展做出了重要贡献.
(1)法国化学家拉瓦锡为化学学科的发展做出了巨大贡献,下列有关发现与他有密切关系的是 .
A.空气的组成
B.质量守恒定律
C.水的组成
D.酸碱指示剂
(2)在密闭容器内加入下列两种物质,并称量加入前后的总质量(含密闭容器),能验证质量守恒定律的 是 (填标号).
A.蔗糖和水
B.氯化钠溶液和硝酸钾溶液
C.氯化钡溶液和稀硫酸
(3)在氧气中点燃红磷的实验过程,固体质量变化如图1所示. ①从燃烧条件分析,固体质量在t1前没有发生变化的原因是 .
②该反应的化学方程式为 .
③参加反应的氧气质量为g.
(4)某学习小组拟在实验室里利用空气和镁粉为原料制取少量氮化镁(Mg3N2). 查阅资料可知Mg、Mg3N2能发生如下反应:
①2Mg+O2 ![]() 2MgO; ②3Mg+N2
2MgO; ②3Mg+N2 ![]() Mg3N2; ③2Mg+CO2
Mg3N2; ③2Mg+CO2 ![]() 2MgO+C
2MgO+C
④Mg+H2O ![]() MgO+H2↑ ⑤Mg3N2+6H2O═3Mg(OH)2↓+2NH3↑
MgO+H2↑ ⑤Mg3N2+6H2O═3Mg(OH)2↓+2NH3↑
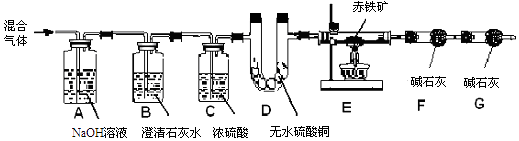
实验中所用的装置和药品如图2所示(镁粉、还原铁粉均已干燥,装置内所发生的反应是完全的,整套装置的末端与干燥管相连).回答下列问题:
①连接并检查实验装置的气密性,实验开始时,将空气通入实验装置,则气流流经装置的顺序是(填装置序号).D装置中发生反应的化学方程式为 .
②通气后,如果同时点燃A、B装置的酒精灯,对实验结果有何影响? .
③设计一个实验,验证产物是否含氮化镁:
实验操作和实验现象 | 实验结论 |
产物中含有氮化镁 |
④思维拓展:空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO的质量却远大于Mg3N的质量,请给出合理的解释 .