题目内容
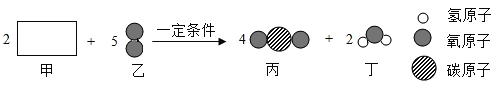
【题目】如图表示某化学反应的微观过程,下列有关说法正确的是 ( )
A.反应前后分子总数不变
B.甲的化学式为C2H2O
C.丙和丁都是氧化物
D.发生反应的甲和乙的质量比为13∶16
【答案】C
【解析】
由化学反应的微观过程及物质的微观构成可知,反应物是乙炔和氧气;由质量守恒定律,生成物是二氧化碳和水,反应的方程式是:2C2H2+5O2 ![]() 4CO2+2H2O,
4CO2+2H2O,
A、2个乙炔分子和5个氧分子在点燃的条件下生成4个二氧化碳分子和2个水分子,反应前后分子总数减少,故选项错误;
B、甲的化学式是C2H2,故选项错误;
C、由两种元素组成,并且其中一种元素是氧元素的化合物叫做氧化物,丙和丁分别是CO2和H2O,属于氧化物,故选项正确;
D、物质的质量比等于化学计量数与物质的相对分子质量之比,甲乙的质量比为13:40,故选项错误。
故选:C。

【题目】某校化学学习小组准备用生石灰制取氢氧化钠固体,他们进行如下探究过程,请根据他们的探究回答问题。
(查阅资料)
温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
NaOH 的溶解度 | 42 | 109 | 129 | 174 | 314 | 147 |
Ca(OH)2 的溶解度 | 0.18 | 0.16 | 0.14 | 0.12 | 0.09 | 0.07 |
(设计实验、制取氢氧化钠)
步骤①:将一定量的生石灰加入一只洁净的烧杯中,加入碳酸钠溶液,充分反应.
步骤②:将所得的混合溶液冷却至室温.
步骤③:将冷却后的混合物过滤、洗涤、干燥得到固体A和溶液B.
(1)过滤操作中,除烧杯和玻璃棒外,过滤必须用到玻璃仪器是____.
(提出问题、假设猜想)
(2)固体A中的成分是什么?
甲同学认为是:CaCO3.
乙同学认为是:CaCO3和Ca(OH)2.
溶液B中溶质的成分是什么?
丙同学认为是:NaOH
丁同学认为是:NaOH、Ca(OH)2
戊同学认为是:____.
(验证猜想、实验探究)
(3)为了验证各自的猜想,甲、乙同学分别进行了实验:
实验步骤 | 实验现象 | 实验结论 |
甲同学:用一支洁净的试管取少量固体A,再加入过量稀盐酸 | ____ | 自己的猜想正确 |
乙同学:用一支洁净的试管取少量的固体A,加水,充分振荡.向上层清液中滴加 ____ | 上层清液由无色变为红色 | 自己的猜想正确 |
(交流表达、反思评价)
(4)同学们经过讨论后认为,甲同学的实验____(填“能”或“不能”)证明固体A的成分,理由是__,最终同学们确定乙同学的猜想是正确的;
(5)同学们得到的固体A8.7g,加入足量的稀盐酸充分反应后,将溶液加热浓缩、蒸发结晶得到11.1g固体,则固体A中所含的CaCO3的质量是____g;
(6)同学们结合对固体成分的探究,经过讨论确定了丁同学对溶液B的猜想正确,理由是___。
(拓展延伸、巩固提高)
(7)同学们欲将溶液B加热浓缩,加热不久,溶液出现浑浊,只好停止加热,请解释加热时溶液出现浑浊的原因是___,于是,同学们立即变换方案,向B溶液中加入适量的____,过滤,将滤液加热浓缩至饱和,____、过滤、洗涤、烘干得到比较纯净的氢氧化钠固体。