题目内容
【题目】过碳酸钠(2Na2CO33H2O2 , 相对分子质量为314)是一种很好的消毒剂和供氧剂,常用于洗涤、印染、纺织、造纸、医药卫生等领域。
Ⅰ.制备过碳酸钠
【查阅资料】过碳酸钠难溶于异丙醇,可浴于水,易发生反应:
2Na2CO33H2O2 =2Na2CO3+3H2O2;碳酸钠与碳酸钙一样也能与盐酸反应放出二氧化碳。
【制备流程】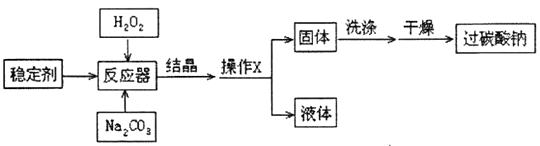
(1)操作X是;
(2)流程中结晶在常温下进行,原因是;
(3)为提高产品的纯度,碳酸钠和过氧化氢的最佳投料质量比是 , 洗涤固体时,选用的最佳试剂是。
(4)II.神奇的“氧立得”
小明同学新买了一台氧立得便携式制氧器,其中有A、B两包固体,B包为黑色固体粉未,经查阅资料知A包主要成分为过碳酸钠。将A包、B包药品分别放入机器,就可以制得氧气。为探究A包固体的纯度,设计了如下图所示实验装置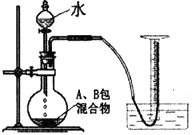
【实验步骤】
①检查装置气密性;
②称取2.2gA包药品和少许B包药品,并全部装入烧瓶内;
③按图搭好装置;④现将橡胶管插入量筒底部;
⑤打开分液漏斗;⑥待反应停止后,保持橡胶管口在量筒底部;
⑦等试管冷却到室温时将橡胶管移出水槽,读取量筒读数为220mL;
⑧数据处理。[氧气在实验条件下密度为1.43g/L]
【问题讨论】
B固体成分为(填化学式),实验时烧瓶内可观察到的现象是
(5)如果将步骤④和⑤对调,实验结果将(选填“偏大”、“偏小”或“不变”),理由题是;
(6)证明反应停止后烧瓶中有碳酸钠的方法是;
(7)此样品中过磺酸钠的质量分数为。
【答案】
(1)过滤
(2)防止过氧化氢分解
(3)106:51,异丙醇
(4)MnO2,有气泡、放热(任意一点即可)
(5)偏小,未将生成的气体全部收集
(6)加入稀盐酸,有气泡产生
(7)93.5%
【解析】Ⅰ.制备过碳酸钠。
(1)操作X是过滤。(2)流程中结晶在常温下进行,原因是防止过氧化氢分解。(3)为提高产品的纯度,碳酸钠和过氧化氢的最佳投料质量比是106:51。洗涤固体时,选用的最佳试剂是异丙醇。
II.神奇的“氧立得”。
【问题讨论】(4)B固体成分MnO2 ,实验时烧瓶内可观察到的现象是. 有气泡、放热。
(5)如果将步骤④和⑤对调,实验结果将偏小,理由是没有将生成的气体全部收集。
(6)证明反应停止后烧瓶中有碳酸钠的方法是加入稀盐酸,有气泡产生。(7)此样品中过碳酸钠的质量分数为∶
生成氧气质量为∶0.220L×1.43g/L=0.32g.
设过氧化氢的质量为x
2H2O2 | O2↑ | ||
68 | 32 | ||
x | 0.32g |
![]() x=0.68g
x=0.68g
设生成0.68g过氧化氢,需过碳酸钠的质量为y
2Na2CO33H2O2 =2Na2CO3+3H2O2
314 102
y 0.68g
![]()
![]() y=2.1g. 此样品中过碳酸钠的质量分数为∶
y=2.1g. 此样品中过碳酸钠的质量分数为∶ ![]() ×100%=93.5%.
×100%=93.5%.
【考点精析】解答此题的关键在于理解过滤操作的注意事项的相关知识,掌握过滤操作注意事项:“一贴”“二低”“三靠;过滤后,滤液仍然浑浊的可能原因有:①承接滤液的烧杯不干净②倾倒液体时液面高于滤纸边缘③滤纸破损,以及对催化剂的特点与催化作用的理解,了解催化剂(触媒):在化学反应中能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质.(一变两不变)催化剂在化学反应中所起的作用叫催化作用.

 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案