题目内容
【题目】钙元素是人体必需的常量元素,分析以下对钙元素的介绍,回答相关问题。

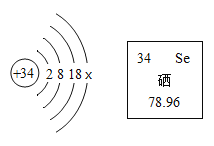
1808年,英国的戴维、瑞典的贝采利乌斯、法国的蓬丁发现了单质钙。如图为钙原子的结构示意图以及钙元素在元素周期表中的单元格。单质化学性质活波,在空气中其表面会形成一层氧化薄膜,以防止单质钙继续受到腐蚀。氧化钙与水反应放出的热量能“煮熟”鸡蛋。人体中的钙主要存在于骨骼和牙齿中。豆制品、干果中含有比较丰富的钙元素。膳食中的钙不能满足人体生理需要时,可摄入补钙药剂。
(1)钙原子的最外层电子数为__________,在化学反应中易_____(填“得到”或“失去”)电子。从钙元素在元素周期表中的单元格可获取的一条信息是______________________________________ 。
(2)单质钙具有很好的抗腐蚀性能,其原因是______。在空气中具有抗腐性能的金属还有_____。(写出一种)
(3)写出氧化钙与水反应的化学方程式______________________________。
【答案】2 失去 钙原子的相对原子质量为40.08 钙在空气中其表面会形成一层氧化薄膜 铝 CaO+H2O === Ca(OH)2
【解析】
解:(1) 由钙元素的原子结构示意图可知,钙原子的最外层有2个电子,在化学反应中易失去最外层的2个电子;由元素周期表的信息可知钙原子的原子序数(或质子数)为20;元素符号为Ca;钙元素是一种金属元素;钙原子的相对原子质量为40.08;
(2) 单质钙化学性质活泼,在空气中其表面会形成一层氧化物薄膜,以防止单质钙继续受到腐蚀,所以单质钙具有很好的抗腐蚀性能;铝在常温下易与空气中的氧气反应生成致密的氧化铝保护膜,对内部结构起到了保护作用;
(3) 氧化钙和水反应的化学方程式为:CaO+H2O═Ca(OH)2。