题目内容
【题目】(4分)莽草酸(化学式:C7H10O5)是制取抗“H1N1流感”药物“达菲”的原料。
请计算:(写出计算过程,并注意格式)
(1)莽草酸分子中C、H、O的质量比;
(2)莽草酸中氢元素的质量分数(精确到0.1%);
(3)174g莽草酸含氢元素的质量:
(4)对1岁以上的儿童推荐按照下列“体重一剂量表”服用“达菲”:
体重 | 小于等于15千克 | 15~23千克 | 23~40千克 | 大于40千克 |
每次用量 | 30mg | 45mg | 60mg | 60mg |
假如患病儿童的体重是35千克,在治疗过程中,需每天服用“达菲”胶囊(每颗胶囊含“达菲”60mg)2次,一个疗程5天,那么该患儿一个疗程共需服用多少颗?
【答案】解:(1)m(C):m(H):m(O)="42:5:" 40
(2)ω(H)=![]() ×100%=
×100%=![]() ×100%=5.7%
×100%=5.7%
(3)m(H)=174g×![]() =10g
=10g
(4)n=![]() =10颗
=10颗
答:略。
【解析】
试题化合物中元素的质量比就等于各元素相对原子质量总和的比;
元素的质量分数=![]() 。
。
(1)C7H10O5中C、H、O的质量比=12×7:1×10:16×5=42:5: 40,即m(C):m(H):m(O)="42:5:" 40
(2)莽草酸中氢元素的质量分数=![]()
=![]() ×100%=
×100%=![]() ×100%=5.7%
×100%=5.7%
(3)174g莽草酸含氢元素的质量=174g×![]() ×100%=10g
×100%=10g
(1) 假如患病儿童的体重是35千克,每天服用“达菲”胶囊2次,每颗胶囊含“达菲”60mg,一个疗程5天,共服用了“达菲”60mg×2×5=600mg,共计600mg/60mg=10颗。
答:略。

 备战中考寒假系列答案
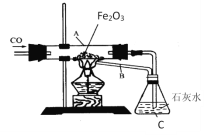
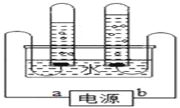
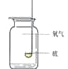
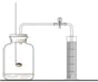
备战中考寒假系列答案【题目】下列实验操作容器中都有水,其解释没有体现水的主要作用的是( )
A | B | C | D | |
实验 装置 |
硫在O2中燃烧 |
测定空气中O2含量 |
铁丝在O2中燃烧 |
探究燃烧条件 |
解释 | 集气瓶中的水:吸收放出的热量 | 量筒中的水:通过水体积的变化得出O2的体积 | 集气瓶中的水:冷却溅落融化物,防止集气瓶炸裂 | 烧杯中的水:加热铜片,隔绝空气 |
A. A B. B C. C D. D