题目内容
利用纯碱在实验室可以制取许多物质,某研究性学习小组对纯碱展开如下探究:Ⅰ.利用纯碱和稀盐酸制取二氧化碳
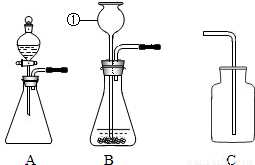
(1)写出如图装置B中标号仪器名称______,用纯碱和稀盐酸制取二氧化碳的反应方程式为______.应该选用的发生装置为______,用装置C收集二氧化
碳导气管需伸到集气瓶底部,目的______.
(2)有人认为用稀硫酸和纯碱制取二氧化碳,优于用稀盐酸和纯碱制取二氧化碳,理由是______.
Ⅱ.利用纯碱和熟石灰制取烧碱溶液
步骤一:将纯碱溶于水,加入适量熟石灰;步骤二:过滤;步骤三:检验滤液中存在的溶质.
(3)步骤一中需要使用玻璃棒,其作用是______,纯碱与熟石灰反应方程式为______.
(4)步骤二中过滤器中滤纸没有紧贴漏斗内壁的后果是______.
(5)小红按下表完成步骤三,请你将小红的实验设计补充完整
| 实验操作 | 实验现象 | 实验结论 | |
| ① | 取少量滤液,滴入纯碱溶液 | 没有白色沉淀产生 | ______ |
| ② | 另取少量滤液,滴入______,静置. | ______ | 含有碳酸钠 和氢氧化钠 |
【答案】分析:此题涉及二氧化碳的实验室制取原理及收集方法的选取,物质的分离与提纯的运用以及物质的鉴定设计、物质的过量反应等等.
解答:解:(1)此小题是用Na2CO3和稀HCl制取二氧化碳,反应原理符合盐和酸生成新盐和新酸的类型;发生装置的选取符合固液不需要加热的反应,故发生装置选A,收集气体时,导气管应深入集气瓶的底部,原因二氧化碳的密度大于空气,目的将原集气瓶中的空气排除;
(2)盐酸和纯碱制取二氧化碳时,因盐酸具有挥发性,致使二氧化碳中会有部分氯化氢气体,使制的二氧化碳不纯;
(3)纯碱溶于水时,玻璃棒不断地搅拌,起到加速物质溶解得作用;纯碱与熟石灰反应属于盐和碱生成新盐和新碱的类型;
(4)若不贴紧,滤纸与漏斗之间就会产生气泡,这有两个后果,①影响过滤速度,②滤液会遇到阻碍从而冲破滤纸,失去过滤效果.③若不贴紧,滤液可能溢出.
(5)此小题是关于物质的过量、剩余的鉴定问题,实验结论的获得取决于加入的物质及发应现象不同.滤液中若含Ca(OH)2,则会出现白色沉淀,加少量氯化钙,即便有碳酸钠溶液剩余也不会出现沉淀,所以应加入过量的氯化钙溶液.
故答案为:(1)长颈漏斗、Na2CO3+2HCl═2NaCl+H2O+CO2↑、A、把空气排净
(2)用盐酸制得的气体中会混有氯化氢气体
(3)加速溶解、Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
(4)过滤速度变慢
(5)滤液中不含Ca(OH)2、过量CaCl2溶液和酚酞试液(无过量不给分)、有白色沉淀产生上层清液呈红色
点评:此题考查了基本的实验操作:物质的制取原理,装置的正确选取,物质的鉴定,复分解化学方程式的书写等知识,学会进行知识间的类比.
解答:解:(1)此小题是用Na2CO3和稀HCl制取二氧化碳,反应原理符合盐和酸生成新盐和新酸的类型;发生装置的选取符合固液不需要加热的反应,故发生装置选A,收集气体时,导气管应深入集气瓶的底部,原因二氧化碳的密度大于空气,目的将原集气瓶中的空气排除;
(2)盐酸和纯碱制取二氧化碳时,因盐酸具有挥发性,致使二氧化碳中会有部分氯化氢气体,使制的二氧化碳不纯;
(3)纯碱溶于水时,玻璃棒不断地搅拌,起到加速物质溶解得作用;纯碱与熟石灰反应属于盐和碱生成新盐和新碱的类型;
(4)若不贴紧,滤纸与漏斗之间就会产生气泡,这有两个后果,①影响过滤速度,②滤液会遇到阻碍从而冲破滤纸,失去过滤效果.③若不贴紧,滤液可能溢出.
(5)此小题是关于物质的过量、剩余的鉴定问题,实验结论的获得取决于加入的物质及发应现象不同.滤液中若含Ca(OH)2,则会出现白色沉淀,加少量氯化钙,即便有碳酸钠溶液剩余也不会出现沉淀,所以应加入过量的氯化钙溶液.
故答案为:(1)长颈漏斗、Na2CO3+2HCl═2NaCl+H2O+CO2↑、A、把空气排净
(2)用盐酸制得的气体中会混有氯化氢气体
(3)加速溶解、Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
(4)过滤速度变慢
(5)滤液中不含Ca(OH)2、过量CaCl2溶液和酚酞试液(无过量不给分)、有白色沉淀产生上层清液呈红色
点评:此题考查了基本的实验操作:物质的制取原理,装置的正确选取,物质的鉴定,复分解化学方程式的书写等知识,学会进行知识间的类比.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
(11分)利用纯碱在实验室可以制取许多物质,某研究性学习小组对纯碱展开如下探究: Ⅰ.利用纯碱和稀盐酸制取二氧化碳
Ⅰ.利用纯碱和稀盐酸制取二氧化碳
(1)写出右图装置B中标号仪器名称 ,用纯
碱和稀盐酸制取二氧化碳的反应方程式为 。
应该选用的发生装置为 ,用装置C收集二氧化
碳导气管需伸到集气瓶底部,目的 。
(2)有人认为用稀硫酸和纯碱制取二氧化碳,优于用稀
盐酸和纯碱制取二氧化碳,理由是 。
Ⅱ.利用纯碱和熟石灰制取烧碱溶液
步骤一:将纯碱溶于水,加入适量熟石灰;步骤二:过滤;步骤三:检验滤液中存在的溶质。
(3)步骤一中需要使用玻璃棒,其作用是 ,纯碱与熟石灰反应方程式为 。
(4)步骤二中过滤器中滤纸没有紧贴漏斗内壁的后果是 。
(5)小红按下表完成步骤三,请你将小红的实验设计补充完整。
| | 实验操作 | 实验现象 | 实验结论 |
| ① | 取少量滤液,滴入纯碱溶液 | 没有白色沉淀产生 | |
| ② | 另取少量滤液,滴入 ,静置。 | | 含有碳酸钠 和氢氧化钠 |
利用纯碱在实验室可以制取许多物质,某研究性学习小组对纯碱展开如下探究:
Ⅰ.利用纯碱和稀盐酸制取二氧化碳
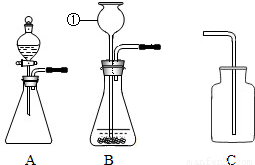
(1)写出如图装置B中标号仪器名称______,用纯碱和稀盐酸制取二氧化碳的反应方程式为______.应该选用的发生装置为______,用装置C收集二氧化
碳导气管需伸到集气瓶底部,目的______.
(2)有人认为用稀硫酸和纯碱制取二氧化碳,优于用稀盐酸和纯碱制取二氧化碳,理由是______.
Ⅱ.利用纯碱和熟石灰制取烧碱溶液
步骤一:将纯碱溶于水,加入适量熟石灰;步骤二:过滤;步骤三:检验滤液中存在的溶质.
(3)步骤一中需要使用玻璃棒,其作用是______,纯碱与熟石灰反应方程式为______.
(4)步骤二中过滤器中滤纸没有紧贴漏斗内壁的后果是______.
(5)小红按下表完成步骤三,请你将小红的实验设计补充完整
Ⅰ.利用纯碱和稀盐酸制取二氧化碳
(1)写出如图装置B中标号仪器名称______,用纯碱和稀盐酸制取二氧化碳的反应方程式为______.应该选用的发生装置为______,用装置C收集二氧化
碳导气管需伸到集气瓶底部,目的______.
(2)有人认为用稀硫酸和纯碱制取二氧化碳,优于用稀盐酸和纯碱制取二氧化碳,理由是______.
Ⅱ.利用纯碱和熟石灰制取烧碱溶液
步骤一:将纯碱溶于水,加入适量熟石灰;步骤二:过滤;步骤三:检验滤液中存在的溶质.
(3)步骤一中需要使用玻璃棒,其作用是______,纯碱与熟石灰反应方程式为______.
(4)步骤二中过滤器中滤纸没有紧贴漏斗内壁的后果是______.
(5)小红按下表完成步骤三,请你将小红的实验设计补充完整
| 实验操作 | 实验现象 | 实验结论 | |
| ① | 取少量滤液,滴入纯碱溶液 | 没有白色沉淀产生 | ______ |
| ② | 另取少量滤液,滴入______,静置. | ______ | 含有碳酸钠 和氢氧化钠 |

 27、利用纯碱在实验室可以制取许多物质,某研究性学习小组对纯碱展开如下探究:
27、利用纯碱在实验室可以制取许多物质,某研究性学习小组对纯碱展开如下探究: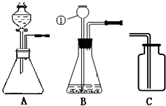 28、利用纯碱在实验室可以制取许多物质,某研究性学习小组对纯碱展 开如下探究:
28、利用纯碱在实验室可以制取许多物质,某研究性学习小组对纯碱展 开如下探究: