题目内容
【题目】将4g含有可溶性杂质的硫酸铜样品溶于足量水,再向所得溶液中逐滴加入75g一定溶质质量分数的氯化钡溶液(杂质不与氯化钡溶液反应)。实验过程中,生成沉淀的质量与滴入氯化钡溶液的质量关系如图所示。试计算:
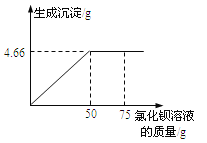
(1)恰好完全反应时,生成沉淀的质量是 g。
(2)样品中硫酸铜的质量分数是多少?
(3)反应后的溶液中,氯化钡的质量是多少?
【答案】(1) 4.66; (2)80% ;(3)2.08g
【解析】
试题分析:(1)有题中的图像可知恰好反应完全时,生成的沉淀的质量为 4.66 g
(2)解:设硫酸铜质量为x、参加反应的氯化钡质量为y、反应后溶液中氯化钡质量为z。
CuSO4 + BaCl2 = BaSO4↓ + CuCl2
160 208 233
x y 4.66g
160/x=233/4.66g 208/y=233/4.66g
x=3.2g y=4.16g
样品中硫酸铜的质量分数为: 3.2g/4g×100%=80%
(3)4.16g/50g×100%×(75g-50g)=2.08g
答:样品中硫酸铜的质量分数是80%,反应后的溶液中,氯化钡的质量为2.08g。

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案
相关题目
