题目内容
【题目】将等质量、颗粒大小相同的X、Y、Z三种金属分别投入到相同浓度的足量的稀硫酸中,生成氢气的质量与时间的关系如图所示。已知它们在化合物中均显+2价,则下列说法不正确的是( )
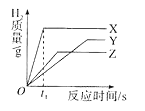
A.在时间为t1时,生成氢气的质量为:X>Z>Y
B.金属活动性:X>Z>Y
C.相对原子质量:X>Y>Z
D.X、Y和Z可能分别是常见金属中的Mg、Fe、Zn
【答案】C
【解析】
试题分析:A、根据图示,在时间为t1时,生成氢气的质量为:X>Z>Y,正确,B、根据反应所需时间越短,说明反应速率越快,金属活动性越强,故金属活动性:X>Z>Y[,正确,C、当金属质量相等,且均形成+2价的化合物,那么生成的氢气质量与金属的相对原子质量成反比,即金属的相对原子质量越大,生成的氢气质量就越小,故根据生成氢气质量关系X>Y>Z,则相对原子质量:Z>Y>X,错误,D、根据上面的分析,金属活动性:X>Z>Y[,相对原子质量:Z>Y>X,故X、Y和Z可能分别是常见金属中的Mg、Fe、Zn,正确,故选C

练习册系列答案
相关题目


