题目内容
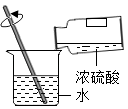
【题目】实验室根据工业炼铁的原理设计了如图所示装置进行实验.请回答:
(1)主要成分为氧化铁的矿石名称为;图中还原氧化铁的化学方程式为:
(2)“加热”和“通气”(通入CO)的操作顺序是 .
【答案】
(1)赤铁矿;3CO+Fe2O3![]() 2Fe+3CO2
2Fe+3CO2
(2)通气、加热
【解析】(1)赤铁矿的主要成分是氧化铁;氧化铁在一氧化碳的高温的条件下反应生成铁和二氧化碳;故填:赤铁矿;3CO+Fe2O3![]() 2Fe+3CO2;(2)因为一氧化碳具有可燃性,能和氧气混合在点燃的条件下会发生爆炸,所以实验开始时应先通一氧化碳再加热,目的是赶尽玻璃管内的空气,防止加热爆炸;故答案为:通气、加热.
2Fe+3CO2;(2)因为一氧化碳具有可燃性,能和氧气混合在点燃的条件下会发生爆炸,所以实验开始时应先通一氧化碳再加热,目的是赶尽玻璃管内的空气,防止加热爆炸;故答案为:通气、加热.
(1)根据炼铁的原料以及反应原理来分析;(2)根据实验的注意事项来分析.本题考查了炼铁的原理以及一氧化碳的可燃性,完成此题,可以依据已有的知识进行,要求同学们加强基础知识的储备,以便灵活应用.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
【题目】过氧化钙(CaO2)是一种环境友好的化工原料,工农业生产中用作漂白剂、种子消毒剂以及鱼类运输时的制氧剂等.过氧化钙与水反应方程式为:2CaO2+2H2O═2Ca(OH)2+O2 .
(1)若用150g某过氧化钙工业样品可制得氧气32g,请计算该过氧化钙样品的纯度(样品中CaO2的质量分数)是多少?
(2)往150g上述过氧化钙工业样品中逐渐加入水至过量,在如图中画出产生氧气的曲线图.
(3)下表为市面上某种过氧化钙和过氧化钠(化学式为Na2O2 , 化学性质与CaO2类似)样品的一些数据:
物质 | 相对分子质量 | 纯度 | 价格(元/kg) |
Na2O2 | 78 | 98% | 25 |
CaO2 | 72 | 94% | 24 |
用3000元购买样品制氧气,请通过计算说明购买哪种产品可制得更多的O2(已知用3000元购买过氧化钙样品可制得26.1kg O2)?