题目内容
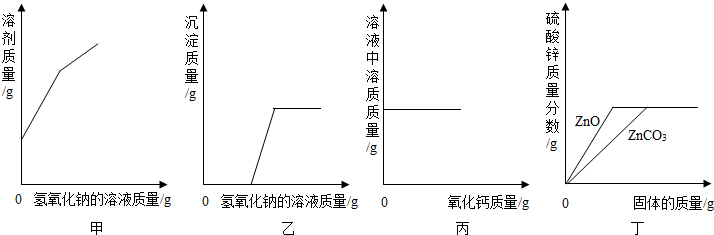
下列四个图象分别对应四种操作过程,其中不正确的是( )
分析:A、根据向NaOH溶液中加入HCl时溶液pH的变化分析;
B、根据向CaCl2溶液中通入CO2时不生成沉分析;
C、根据加入NaOH时溶液发生的反应,NaOH首先是和盐酸发生反应,没有沉淀产生,继续加NaOH溶液才和CuCl2反应,生成沉淀分析;
D、由于Mg比Fe活泼,所以二者和盐酸反应速度不一样,Mg反应要快.
B、根据向CaCl2溶液中通入CO2时不生成沉分析;
C、根据加入NaOH时溶液发生的反应,NaOH首先是和盐酸发生反应,没有沉淀产生,继续加NaOH溶液才和CuCl2反应,生成沉淀分析;
D、由于Mg比Fe活泼,所以二者和盐酸反应速度不一样,Mg反应要快.
解答:解:A、NaOH溶液显碱性,起点时溶液pH大于7,加入HCl发生的反应为NaOH+HCl=NaCl+H2O,正好反应时为中性溶液,pH为7,盐酸过量时pH小于7.所以A图象正确;
B、CaCl2溶液和CO2不会发生反应,不能生成沉淀,所以B图象错误;
C、加入NaOH溶液首先发生反应NaOH+HCl=NaCl+H2O,没有沉淀产生,继续加NaOH溶液发生反应CuCl2+2NaOH=Cu(OH)2↓+2NaCl,生成Cu(OH)2沉淀,当NaOH过量时不溶解,所以C图象正确;
D、发生的反应为Fe+2HCl=FeCl2+H2↑,Mg+2HCl=MgCl2+H2↑,因为加入的盐酸质量相等,Mg和Fe足量,根据化学方程式可知生成的H2质量相等,但由于Mg比Fe活泼,所有Mg和盐酸首先反应完,所用时间少,所以D图象正确.
故选B.
B、CaCl2溶液和CO2不会发生反应,不能生成沉淀,所以B图象错误;
C、加入NaOH溶液首先发生反应NaOH+HCl=NaCl+H2O,没有沉淀产生,继续加NaOH溶液发生反应CuCl2+2NaOH=Cu(OH)2↓+2NaCl,生成Cu(OH)2沉淀,当NaOH过量时不溶解,所以C图象正确;
D、发生的反应为Fe+2HCl=FeCl2+H2↑,Mg+2HCl=MgCl2+H2↑,因为加入的盐酸质量相等,Mg和Fe足量,根据化学方程式可知生成的H2质量相等,但由于Mg比Fe活泼,所有Mg和盐酸首先反应完,所用时间少,所以D图象正确.
故选B.
点评:本题是图象与反应的考查题,在处理图象类问题时,曲线的起点、折点及变化趋势是进行判断的要点.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目
下列四个图象分别对应四种操作过程,其中不正确的是( )
A、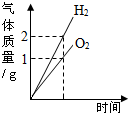 甲--电解水 | B、 乙--向盐酸和氯化钙的混合溶液中滴加碳酸钠溶液 | C、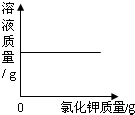 丙--在室温下,向一定量的食盐饱和溶液中不断加入氯化钾晶体 | D、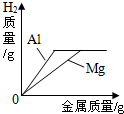 丁--向等质量、等质量分数的稀硫酸中分别加入镁和铝 |