题目内容
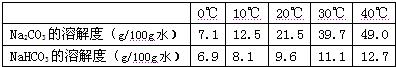
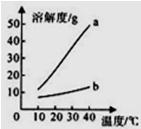
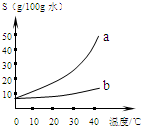 以下是Na2CO3、NaHCO3的溶解度表及溶解度曲线.
以下是Na2CO3、NaHCO3的溶解度表及溶解度曲线.(1)Na2CO3溶解度曲线为
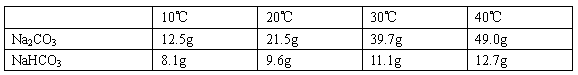
| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | |
| Na2CO3的溶解度(g/100g水) | 7.1 | 12.5 | 21.5 | 39.7 | 49.0 |
| NaHCO3的溶解度(g/100g水) | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 |
①冷却热饱和溶液 ②蒸发溶剂 ③溶解过滤
(3)已知Na2CO3转化为NaHCO3的反应为Na2CO3+CO2+H2O→2NaHCO3,根据以上信息,要除去NaHCO3饱和溶液中的少量Na2CO3,应采用的化学方法是
(4)40℃时的100g Na2CO3的饱和溶液中含有
(5)若将30%的碳酸钠溶液100g,稀释到10%,需要加水
分析:(1)由Na2CO3、NaHCO3的溶解度表及溶解度曲线,则可知:Na2CO3溶解度曲线为变化趋势大的.
(2)由Na2CO3、NaHCO3的溶解度曲线图,可知要除去Na2CO3固体中的少量NaHCO3,应采用的物理方法;
(3)已知Na2CO3转化为NaHCO3的反应为Na2CO3+CO2+H2O→2NaHCO3,根据以上信息,要除去NaHCO3饱和溶液中的少量Na2CO3,应采用的化学方法是让碳酸钠与二氧化碳反应.
(4)由Na2CO3、NaHCO3的溶解度表,可知40℃时碳酸钠的溶解度,则可求100gNa2CO3的饱和溶液中含有溶质的质量,可求该溶液的溶质质量分数;
(5)若将30%的碳酸钠溶液100g,稀释到10%,根据稀释前后溶质的质量相等,可求需要加水的质量.
(2)由Na2CO3、NaHCO3的溶解度曲线图,可知要除去Na2CO3固体中的少量NaHCO3,应采用的物理方法;
(3)已知Na2CO3转化为NaHCO3的反应为Na2CO3+CO2+H2O→2NaHCO3,根据以上信息,要除去NaHCO3饱和溶液中的少量Na2CO3,应采用的化学方法是让碳酸钠与二氧化碳反应.
(4)由Na2CO3、NaHCO3的溶解度表,可知40℃时碳酸钠的溶解度,则可求100gNa2CO3的饱和溶液中含有溶质的质量,可求该溶液的溶质质量分数;
(5)若将30%的碳酸钠溶液100g,稀释到10%,根据稀释前后溶质的质量相等,可求需要加水的质量.
解答:解:
(1)由Na2CO3、NaHCO3的溶解度表及溶解度曲线,则可知:Na2CO3溶解度曲线为a.
(2)由图可知,要除去Na2CO3固体中的少量NaHCO3,应采用的物理方法是:冷却热饱和溶液,故选①;
(3)已知Na2CO3转化为NaHCO3的反应为Na2CO3+CO2+H2O→2NaHCO3,根据以上信息,要除去NaHCO3饱和溶液中的少量Na2CO3,应采用的化学方法是:通入过量二氧化碳.因为碳酸钠溶液与二氧化碳反应生成碳酸氢钠;
(4)由表可知,40℃时碳酸钠的溶解度为49.0克,则100gNa2CO3的饱和溶液中含有100×
×100%=32.9g溶质,该溶液的溶质质量分数为
×100%=32.9%;
(5)若将30%的碳酸钠溶液100g,稀释到10%,因为稀释前后溶质的质量相等,设加水的质量为x,则100×30%=(100+x)×10%,故x=200克,则可知需要加水200mL.
故答为:(1)a;(2)①;(3)通入过量二氧化碳.
(4)32.9g; 32.9%;(5)200ml.
(1)由Na2CO3、NaHCO3的溶解度表及溶解度曲线,则可知:Na2CO3溶解度曲线为a.
(2)由图可知,要除去Na2CO3固体中的少量NaHCO3,应采用的物理方法是:冷却热饱和溶液,故选①;
(3)已知Na2CO3转化为NaHCO3的反应为Na2CO3+CO2+H2O→2NaHCO3,根据以上信息,要除去NaHCO3饱和溶液中的少量Na2CO3,应采用的化学方法是:通入过量二氧化碳.因为碳酸钠溶液与二氧化碳反应生成碳酸氢钠;
(4)由表可知,40℃时碳酸钠的溶解度为49.0克,则100gNa2CO3的饱和溶液中含有100×
| 49 |
| 149 |
| 49 |
| 149 |
(5)若将30%的碳酸钠溶液100g,稀释到10%,因为稀释前后溶质的质量相等,设加水的质量为x,则100×30%=(100+x)×10%,故x=200克,则可知需要加水200mL.
故答为:(1)a;(2)①;(3)通入过量二氧化碳.
(4)32.9g; 32.9%;(5)200ml.
点评:掌握固体溶解度曲线及其作用;了解混合物的分离方法和用水稀释改变浓度的方法.

练习册系列答案
相关题目
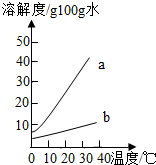 以下是Na2CO3、NaHCO3的溶解度表及溶解度曲线.
以下是Na2CO3、NaHCO3的溶解度表及溶解度曲线.(1)Na2CO3溶解度曲线为
| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | |
| Na2CO3的溶解度(g/100g水) | 7.1 | 12.5 | 21.5 | 39.7 | 49.0 |
| NaHCO3的溶解度(g/100g水) | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 |
Ⅰ.冷却结晶Ⅱ.蒸发结晶Ⅲ.溶解过滤
(3)已知Na2CO3转化为NaHCO3的反应为Na2CO3+CO2+H2O→2NaHCO3,根据以上信息,要除去NaHCO3饱和溶液中的少量Na2CO3,应采用的化学方法是
(4)40℃时的100.0g Na2CO3的饱和溶液中含有

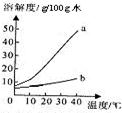 6、以下是Na2CO3、NaHCO3的溶解度表及溶解度曲线.
6、以下是Na2CO3、NaHCO3的溶解度表及溶解度曲线.