题目内容
一定质量的镁条在氧气中完全燃烧后生成氧化镁.固体质量随时间的变化关系如图所示.下列说法不正确的是( )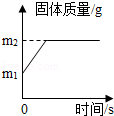
| A.生成MgO的质量:m2g |
| B.参加反应的Mg的质量:m1 g |
| C.参加反应的O2的质量:(m2﹣m1)g |
D.参加反应的镁和氧气的质量比=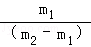 |
D
解析试题分析:A、由图象可知反应的最后固体质量最终为m2g,该值即是氧化镁的质量;
B、该反应的期初固体的质量即为镁的质量,所以为m1 g;
C、由于氧化镁的质量等于镁和参加反应的氧气的质量和,所以参加反应的O2的质量:(m2﹣m1)g;
D、由镁的燃烧的方程式为2Mg+O2 2MgO可知镁和氧气的质量比为
2MgO可知镁和氧气的质量比为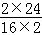 =,利用BC的结论可知镁和氧气的质量比=
=,利用BC的结论可知镁和氧气的质量比=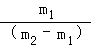 ;
;
故选D
考点:根据化学反应方程式的计算.
点评:运用质量守恒定律时,一定不能漏掉反应物或生成物的质量,特别是气体物质的质量.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
某钢样品的含碳量为0.6%(杂质元素不考虑),若碳元素主要以Fe2C和Fe3C的形式存在,则该钢样品中Fe2C和Fe3C的质量分数(ω)范围是( )
| A.0.03%<ω<2% | B.0.6%<ω<0.87% |
| C.2.48%<ω<3.6% | D.6.2%<ω<9% |
某NaOH固体样品已部分变质。常温下,取61.2g该样品溶于水得到1000g溶液,取出500g溶液进行测定,其中含Na元素16.1g,碳元素1.2g,则原NaOH固体样品中NaOH的质量分数为
| A.65.4% | B.34.6% | C.82.3% | D.64.5% |
(7分) 小明将14.4g含杂质的纯碱样品(碳酸钠与氯化钠的混合物)与90g稀盐酸相混合,恰好完全反应,测得反应生成气体的质量(m)与反应时间(t)的数据如下表所示:
| 反应时间t/s | t0 | t1 | t2 | t3 | t4 | t5 | t6 | t 7 |
| 气体质量m/g | 0 | 0.88 | 1.76 | 2.64 | 3.52 | 4.4 | X | 4.4 |
计算样品中NaCl的质量;
计算完全反应后所得溶液中溶质的质量分数