题目内容
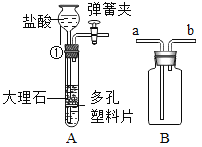
【题目】为加深对一氧化碳还原性的理解,减少一氧化碳对环境的污染,某同学设计了如图所示的实验:
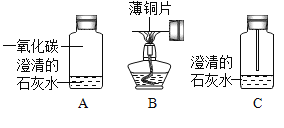
回答下列问题。
(1)图B中,薄铜片受热时发生反应的化学方程式为__________。
(2)趁热将图B所示的薄钢片插入到图A所示的装置中(如图C所示),观察薄铜片的颜色变化,现象是________。
(3)实验结束后用燃着的木条点燃瓶中剩余的气体,有明显的蓝色火焰出现,该反应的化学方程式为__________。
【答案】2Cu+O2![]() 2CuO 铜丝由黑色变红 2CO+O2
2CuO 铜丝由黑色变红 2CO+O2![]() 2CO2
2CO2
【解析】
(1)图B中,薄铜片受热时与氧气反应生成了氧化铜,发生反应的化学方程式为:2Cu+O2![]() 2CuO。
2CuO。
(2)趁热将图B所示的薄铜片插入到图A所示的装置中,氧化铜被一氧化碳还原为铜和二氧化碳,二氧化碳能与氢氧化钙反应生成了碳酸钙和水,所以观察簿铜片的颜色变化,现象是由黑色变成红色;振荡集气瓶,观察到的现象是:澄清的石灰水变浑浊。
(3)实验结束后用燃着的木条点燃瓶中的剩余气体,有明显的蓝色火焰出现,这是一氧化碳燃烧生成了二氧化碳,该反应的化学方程式为2CO+O2![]() 2CO2。
2CO2。

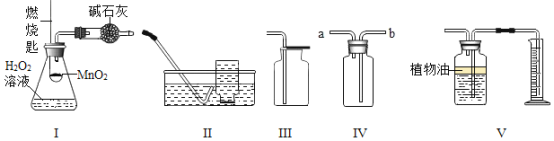
【题目】某同学发现一瓶没有塞上瓶塞的过氧化氢溶液,对该溶液中是否有过氧 化氢的剩余,与同学们一起进行如下探究实验。
(猜想与假设)猜想(1):该溶液中有过氧化氢的剩余。猜想(2):该溶液中没有过氧化氢的剩余。
(方案讨论)为了验证猜想,甲、乙、丙三同学分别提出如下方案:
甲:取适量试剂于试管中,伸入带火星的木条,若带火星的木条复燃,则猜想(1)成立,若带火星的木条不复燃,猜想(2)成立。
同学们认为此方案不行,原因是_____。
乙:取少量二氧化锰于试管中,加入与甲等量的试剂,若有气泡产生,则猜想(1)成立,若无气泡产生则猜想(2)成立,理由是___________________(写化学反应的符号表达式)
丙:
操作 | 现象 | 结论 |
取与甲同学等量的试剂于另一支试 管中,加热,再伸入带火星的木条 | ______________________________________, _______________________________________ | 猜想Ⅰ成立 |
(反思与交流)(1)敞口放置的试剂容易变质,所以要_____保存。
(2)二氧化锰在过氧化氢的分解过程中起_________作用。除此之外能改变化学反应速率的方法还可以_____