题目内容
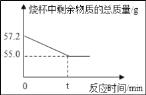
【题目】为测定某地石灰石样品中碳酸钙的质量分数,进行以下实验;向装有10.0g 石灰石样品的烧杯中,加入47.2g稀盐酸,恰好完全反应,烧杯中剩余物质的总质量随时间变化关系如图所示(石灰石中的杂质不参加反应且难溶于水),试计算:
(1)完全反应时生成二氧化碳的质量为_____g;
(2)样品中碳酸钙的质量分数_____。
【答案】2.2 50%
【解析】
碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,反应前后的质量差即为反应生成二氧化碳的质量,根据二氧化碳质量可以计算碳酸钙的质量,进一步可以计算石灰石中碳酸钙的质量分数。
解:(1)生成CO2的质量为:10.0g+47.2g﹣55g=2.2g,
(2)设石灰石样品中碳酸钙的质量为x,
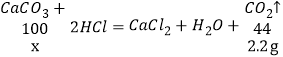
![]() ,
,
x=5g,
石灰石中碳酸钙的质量分数为:![]() ×100%=50%。
×100%=50%。
答:石灰石中碳酸钙的质量分数为50%。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目