题目内容
【题目】(17分)某兴趣小组根据实验室提供的仪器和药品(氯酸钾和二氧化锰)进行了氧气的制备实验。


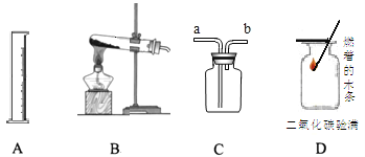
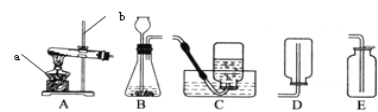
(1)写出图乙中各仪器的名称(任意写出5种):
________、________、________、________、________;
(2)制取氧气应选用的装置是________(填“甲”或“乙”),收集氧气可用________法和________法。此反应的文字表达式为:____________________________________。
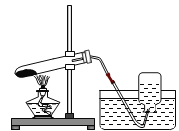
(3)木炭在图丁中燃烧的现象是______________________________________。图戊中的现象为________________________________,说明木炭燃烧的产物有____________。
(4)木炭燃烧这个反应的文字表达式为:__________________________________。

 【答案】(1)试管、铁架台、酒精灯、橡胶塞、导管、试管夹、小木块、铁夹 (2)乙、排水、向上排空气;氯酸钾
【答案】(1)试管、铁架台、酒精灯、橡胶塞、导管、试管夹、小木块、铁夹 (2)乙、排水、向上排空气;氯酸钾![]() 氯化钾+氧气; (3)发白光,放出热量;澄清石灰水变浑浊;二氧化碳(1分)(4)碳+氧气
氯化钾+氧气; (3)发白光,放出热量;澄清石灰水变浑浊;二氧化碳(1分)(4)碳+氧气![]() 二氧化碳 。
二氧化碳 。
【解析】
试题分析:根据题中的装置图可知,(1)各仪器的名称为试管、铁架台、酒精灯、橡胶塞、导管、试管夹、小木块、铁夹;(2)因为用氯酸钾和二氧化锰制取氧气,故选择乙装置,收集氧气可用排水法和向上排空气法,反应的文字表达式为氯酸钾![]() 氯化钾+氧气;(3)木炭在图丁中燃烧的现象是发白光,放出热量;图戊中的现象为澄清石灰水变浑浊;说明木炭燃烧的产物有二氧化碳;(4)木炭燃烧这个反应的文字表达式为碳+氧气
氯化钾+氧气;(3)木炭在图丁中燃烧的现象是发白光,放出热量;图戊中的现象为澄清石灰水变浑浊;说明木炭燃烧的产物有二氧化碳;(4)木炭燃烧这个反应的文字表达式为碳+氧气![]() 二氧化碳 。
二氧化碳 。

 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案【题目】某兴趣小组同学对实验室制备氧气的条件进行如下探究实验.
【提出问题】①氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计并完成实验】
Ⅰ.将3.0g氯酸钾放在试管中加热
Ⅱ.将3.0g氯酸钾与1.0g二氧化锰均匀混合加热
Ⅲ.将x g氯酸钾与1.0g氯化铜均匀混合加热
【实验现象分析】
Ⅲ中x的值应为 ,将实验Ⅰ和Ⅲ比较可证明 ,将实验Ⅲ反应后的固体加水溶解、过滤、洗涤、干燥,若称量得到1.0g黑色粉末,再将黑色粉末和xg氯酸钾混合加热,现象与实验Ⅲ相同,此步骤是为了证明氧化铜在该化学反应前后 和 都不变.
【结论】氧化铜还能作氯酸钾分解的催化剂,请写出实验Ⅲ中的化学反应文字表达式
【实验反思】实验Ⅱ和Ⅲ对比是为了证明
【提出问题】②双氧水分解速度还和什么因素有关
【设计并完成实验】
双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生产生O2体积 | |
Ⅰ | 50.0g | 1% | 0.1g | 9mL |
Ⅱ | 50.0g | 2% | 0.1g | 16mL |
Ⅲ | 50.0g | 4% | 0.1g | 31mL |
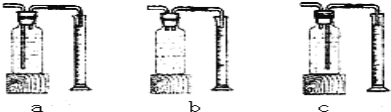
本实验中,测量O2体积的装置是 (填编号)
【结论】在相同条件下,双氧水的浓度越大,双氧水分解得越 。