题目内容
下面为元素周期表的一部分.下列叙述错误的是( )
| ||||||||||||||||||||||||||||||||||||||||
分析:A、根据在原子中,原子序数=质子数=核外电子数=核电荷数分析;
B、元素周期表中每一个周期都从金属元素开始,到稀有气体元素结束(第一周期从非金属元素氢开始).稀有气体元素,原子最外层电子数为8(氦为2 ),为稳定结构;
C、原子结构示意图的特点:非金属元素的最外层电子数一般多于4,易得到电子,形成阴离子;当核电荷数=质子数<核外电子数,为阴离子;
D、原子结构示意图的特点:金属元素的最外层电子数一般少于4,易失去最外层电子形成阳离子.
B、元素周期表中每一个周期都从金属元素开始,到稀有气体元素结束(第一周期从非金属元素氢开始).稀有气体元素,原子最外层电子数为8(氦为2 ),为稳定结构;
C、原子结构示意图的特点:非金属元素的最外层电子数一般多于4,易得到电子,形成阴离子;当核电荷数=质子数<核外电子数,为阴离子;
D、原子结构示意图的特点:金属元素的最外层电子数一般少于4,易失去最外层电子形成阳离子.
解答:解:A、根据在原子中,原子序数=质子数=核外电子数=核电荷数,因此钙的核电荷数是20,故A说法正确;
B、根据元素周期表中每一个周期都从金属元素开始,到稀有气体元素结束(第一周期从非金属元素氢开始). 稀有气体元素,原子最外层电子数为8(氦为2 ),为稳定结构,因此每个周期结尾元素的化学性质比较稳定,故B说法正确;
C、根据原子结构示意图的特点:非金属元素的最外层电子数一般多于4,易得到电子,形成最外层8电子的稳定结构;而图中核电荷数=质子数=核外电子数,为原子结构,故C说法错误;
D、根据原子结构示意图的特点:金属元素的最外层电子数一般少于4,易失去最外层电子形成阳离子;因此镁在化学反应中较易失去电子,故D说法正确;
故选C.
B、根据元素周期表中每一个周期都从金属元素开始,到稀有气体元素结束(第一周期从非金属元素氢开始). 稀有气体元素,原子最外层电子数为8(氦为2 ),为稳定结构,因此每个周期结尾元素的化学性质比较稳定,故B说法正确;
C、根据原子结构示意图的特点:非金属元素的最外层电子数一般多于4,易得到电子,形成最外层8电子的稳定结构;而图中核电荷数=质子数=核外电子数,为原子结构,故C说法错误;
D、根据原子结构示意图的特点:金属元素的最外层电子数一般少于4,易失去最外层电子形成阳离子;因此镁在化学反应中较易失去电子,故D说法正确;
故选C.
点评:本题考查学生对原子结构示意图的特点和元素周期律知识的理解与掌握,并能在解题中灵活应用的能力.

练习册系列答案
 每课必练系列答案
每课必练系列答案
相关题目
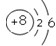
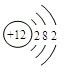 元素周期表是我们学习和研究化学的重要工具,它的内容十分丰富.下面是元素周期表部分内容,请回答下列问题:
元素周期表是我们学习和研究化学的重要工具,它的内容十分丰富.下面是元素周期表部分内容,请回答下列问题: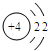 B.
B.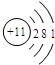 C.
C.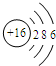 D.
D.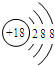

 ,当x-y=8时,该粒子符号为
,当x-y=8时,该粒子符号为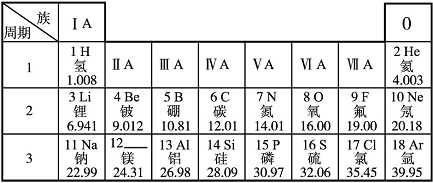
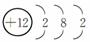 ,在化学反应中该原子易______(填“得到”或“失去”)电子。
,在化学反应中该原子易______(填“得到”或“失去”)电子。