题目内容
【题目】为探究酸、碱、盐的化学性质,某兴趣小红做了如下实验。
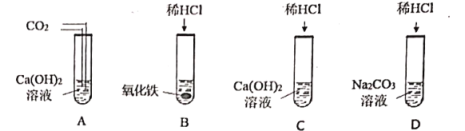
试回答下列问题
(1)试管A中的现象是_____,试管B反应后溶液呈_____色。
(2)该兴趣小组使用的五种实验药品,若两两相互滴加,可以发生的复分解反应有_____个。
(3)实验结束后.该兴趣小组将四支试管中的废液倒入一只洁净的烧杯中充分反应后,观察到黄色澄清溶液,则反应后的废液中可能存在的离子有_____(填离子符号)
【答案】澄清石灰水变浑浊 黄 4 H+
【解析】
(1)试管A中是氢氧化钙和二氧化碳的反应,会生成白色沉淀碳酸钙和水,故实验现象是:澄清石灰水变浑浊,试管B盐酸和氧化铁反应生成氯化铁和水,氯化铁为黄色溶液,故反应后溶液呈黄色。故填:澄清石灰水变浑浊;黄
(2)该兴趣小组使用的五种实验药品分别是二氧化碳、氢氧化钙、氧化铁、稀盐酸、碳酸钠,若两两相互滴加,先判断能否发生反应再判断反应类型,两两混合组合有10个,可以发生反应的有5个,其中属于复分解反应的有4个。
(3)实验结束后,该兴趣小组将四支试管中的废液倒入一只洁净的烧杯中充分反应后,观察到黄色溶液,可知溶液里肯定有铁离子,澄清溶液说明没有沉淀,可知溶液可能为酸性或中性,若为碱性则会有氢氧化铁沉淀。故反应后的废液中可能存在的离子有H+。故填:H+

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
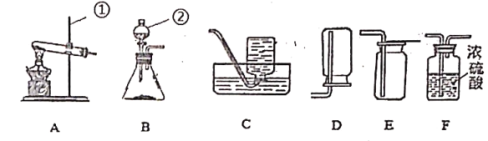
【题目】看图并请从A或B两题中任选1个作答,若两题均作答,只一组计分。
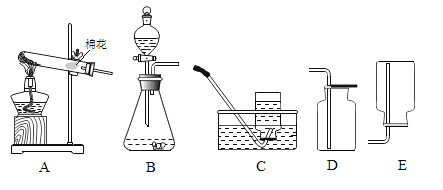
A | B |
(1)用装置A制备一瓶氧气,其制备原理为_____(写出化学反应的方程式)。 (2)氧气可用C装置收集,还可以用__收集(填写装置编号)。 | (1)装置B可用于实验室制取二氧化碳。写出制取CO2反应的化学方程式为__。 (2)收集二氧化碳可选择___(填写装置编号)。 |