题目内容
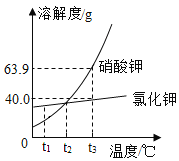
【题目】根据如图中的硝酸钾和氯化钠的溶解度曲线,回答下列问题:
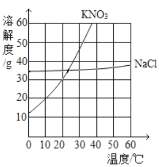
(1)10℃时,将15g硝酸钾加入到l00g水中,充分溶解后,得到硝酸钾的______(选填“饱和”或“不饱和溶液)
(2)30℃时,硝酸钾饱和溶液和氯化钠饱和溶液各100g,分别蒸发掉10g水,恢复至30℃时,______饱和溶液析出的晶体较多
(3)氯化钠溶液中含有少量硝酸钾,提纯氯化钠,采用的方法是______(选填“蒸发结晶”或“降温结晶”)
【答案】不饱和 KNO3 蒸发结晶
【解析】
(1)10℃时,硝酸钾的溶解度为20g,故为不饱和溶液;
(2)30℃时硝酸钾的溶解度大于氯化钠,故蒸发掉等质量的水时,硝酸钾析出的晶体较多;
(3)由于氯化钠的溶解度随温度变化不大,故用蒸发结晶的方法提纯氯化钠。
故答案为:不饱和;KNO3;蒸发结晶

练习册系列答案
相关题目
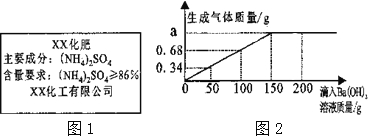
【题目】小红称取5.0g某品牌化肥(商标如图1)于烧杯中,加水完全溶解,滴入Ba(OH)2溶液进行该化肥中(NH4)2SO4含量的测定(杂质溶于水但不参加反应)。测定数据如表和图2所示。
滴入Ba(OH)2溶液质量/g | 50 | 100 | 150 | 200 |
生成沉淀质量/g | 2.33 | 4.66 | 6.99 | m |
已知:(NH4)2SO4+Ba(OH)2═BaSO4↓+2NH3↑+2H2O
(1)表格中的m、坐标上的a数值分别为 ____、____;
(2)该化肥属于____(填“合格”或“不合格”)产品
(3)计算所用Ba(OH)2溶液中溶质的质量分数____(写出计算过程,结果精确至0.01%)。