题目内容
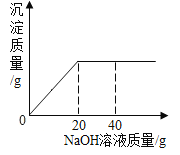
【题目】往10g硫酸和硫酸铜的混合溶液中,逐滴加入溶质质量分数为10%的氢氧化钠溶液,所得溶液的质量和加入的氢氧化钠溶液质量关系如图所示。下列说法错误的是( )
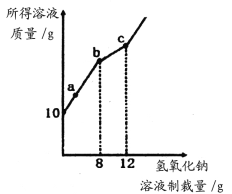
A.a点时溶液中有3种溶质
B.b点时溶液中水的质量为15.78g
C.c点时溶液的pH=7
D.原混合溶液中硫酸铜的质量分数为16%
【答案】D
【解析】
硫酸和氢氧化钠反应生成硫酸钠和水,硫酸铜和氢氧化钠反应生成硫酸钠和氢氧化铜蓝色沉淀。
A、氢氧化钠先和硫酸反应生成硫酸钠和水,a点时溶液中溶质为硫酸钠、氢氧化钠、硫酸铜3种溶质,故A正确;
B、氢氧化钠和硫酸、硫酸铜反应的化学方程式及其质量关系为
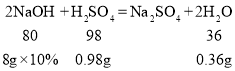
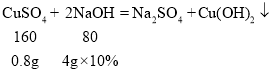
则10g硫酸和硫酸铜的混合溶液中水的质量为![]() ,b点反应时生成水的质量为0.36g,则b点时溶液中水的质量为
,b点反应时生成水的质量为0.36g,则b点时溶液中水的质量为![]() ,8g氢氧化钠溶液中水的质量为8g-8g×10%=7.2g,则b点溶液中水的质量为7.2g+8.58g=15.78g,故B正确;
,8g氢氧化钠溶液中水的质量为8g-8g×10%=7.2g,则b点溶液中水的质量为7.2g+8.58g=15.78g,故B正确;
C、c点时氢氧化钠和硫酸、硫酸铜刚好完全反应,溶液的pH=7,故C正确;
D、原混合溶液中硫酸铜的质量分数为![]() 。故D不正确。故选D。
。故D不正确。故选D。

 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案【题目】某学习小组的同学前往当地的石灰石矿区进行调查,他们取了若干块矿石样品,对样品中的碳酸钙的质量分数进行检测,采用了以下的办法:取用12. 0g这种石灰石样品,把40.0g稀盐酸分四次加入,测量过程所得数据见下表(杂质不溶于水,不与盐酸反应)。
序号 | 第一次 | 第二次 | 第三次 | 第四次 |
加入稀盐酸质量(g) | 10.0 | 10.0 | 10.0 | 10.0 |
剩余固体质量(g) | 8.0 | m | 2.0 | 2.0 |
请计算: (1) 表中的m的数值应为_____;
(2)样品中的碳酸钙的质量分数是_____;
(3)产生二氧化碳的总质量是多少?_____
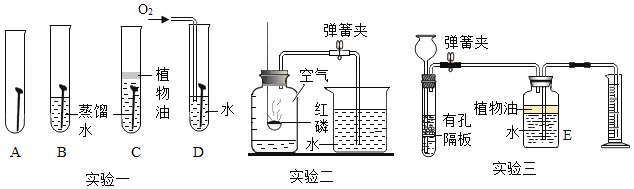
【题目】下图是实验室制取气体的部分装置,请回答:
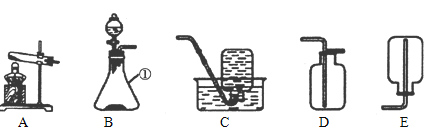
(1)图中仪器①的名称是_________。装置B中使用分液漏斗的优点是________。
(2)实验室用高锰酸钾制取氧气可选用的发生装置是______(填序号);发生反应的化学方程式为___________________。
(3)小组同学对带火星的木条复燃是否需要纯氧产生疑问,开展如下实验:
集气瓶编号 | 1 | 2 | 3 | 4 |
集气瓶中氧气的含量% | 30 | 40 | 50 | 60 |
带火星的木条 | 亮 | 很亮 | 复燃 | 复燃 |
①该小组同学收集氧气时应该选用收集装置是________(填序号)。
②设置4组实验,且每次用同一根木条插入相同的深度,这样做的目的是________。
③欲探究木条复燃所需氧气含量更精确的数值,请写出简要实验方案______。
【题目】物质的组成、结构、性质与制备
(1)物质的组成和结构决定了物质的性质。请你利用已有的化学知识完成下表并填空
物质的名称(或俗称) | 构成物质的微粒符号 | 体现物质化学性质的变化(用方程式表示,写一个即可) |
_________ | Na+、OH- | _________ |
乙醇 | _________ | _________ |
铜 | _________ | _________ |
上表你列举的体现物质化学性质的反应中,包含的基本反应类型有______。
(2)利用物质的性质可以检验或鉴别物质。实验室有一瓶失去标鉴的溶液,为了鉴别其是稀盐酸还是氯化镁溶液,小组同学选用不同的试剂进行实验,都将其鉴别了出来。
可供选择的试剂:银片、生锈的铁钉、块状石灰石、二氧化碳、硝酸银溶液、澄清的石灰水
请按要求填写下表(只填写检验过程中可观察到明显现象的化学变化方程式)
检验过程中发生化学变化的方程式 | 运用物质的性质 |
_________ | 盐能与某些碱反应 |
_________ | _________ |
_________ | _________ |
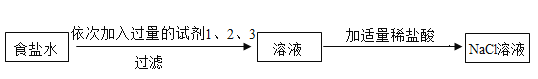
(3)利用物质的性质可通过化学变化制备物质胆矾(CuSO4·5H2O)在工农业生产中有广泛的用途。实验室利用废旧电池的铜棒(主要含铜和锌)为原料制备胆矾。实验流程如图所示:查阅资料:氧化锌能溶于氢氧化钠溶液。
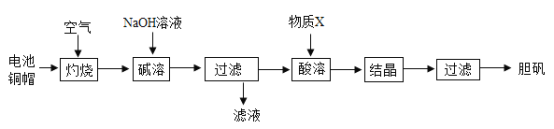
①废旧电池钢帽的表面常有油污,可用洗洁精预先除去,洗洁精在除去油污的过程中起____________作用。
②“碱溶”步骤中,为加快反应速率可采取多种措施,如搅拌、______、______等。
③“酸溶”时,发生反应的化学方程式是_____________。
④试写出胆况在工农业生产中的一种用途_______________.