题目内容
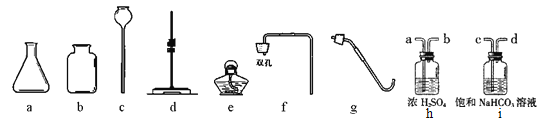
【题目】以下是在实验室里制备二氧化碳气体的实验仪器和装置:
(1)实验室制取CO2的化学方程式为CaCO3 + 2HCl ==CaCl2 + CO2↑ + H2O
①若要制取4.4g CO2,至少需要 g 含CaCO380%的大理石;
②组装一套实验室制取二氧化碳的装置,选用的仪器有a、b、f和 ;
③实验室制得的CO2中常含有HCl和水蒸气。为了得到纯净、干燥的CO2,可选用装置h和i进行除杂,导管的连接顺序是 (用导管口的序号表示),发生反应的化学方程式是 ;
(2)实验室常用无水醋酸钠固体与碱石灰固体在加热的条件下制取CH4,发生装置除了选用上述部分仪器外,还必须补充的玻璃仪器是 。
【答案】(1)①12.5g ②c ③c、d、a、b ,NaHCO3+HCl=NaCl+H2O+CO2↑(2)试管
【解析】
试题分析:(1)①利用反应的化学方程式,根据反应的质量比即可计算出碳酸钙的质量。
设碳酸钙的质量为x;
CaCO3+2HCl=CaCl2+CO2↑+H2O
100 44
X 4.4g
100/44 =x/4.4g x=10g
需要含碳酸钙80%的大理石的质量=10g÷80% =12.5g ;
②实验室用石灰石或大理石和稀盐酸反应制取二氧化碳,属固液在常温下的反应,故还需要长颈漏斗,选c;
③要得到纯净的二氧化碳,那么要先除杂再干燥,即氯化氢气体用饱和的碳酸氢钠溶液除去,水蒸气用浓硫酸除去。在除杂和干燥的过程中,一定要使气体与药品充分接触,故连接顺序是:c、d、a、b;碳酸氢钠与稀盐酸反应生成氯化钠、水和二氧化碳:NaHCO3+HCl=NaCl+H2O+CO2↑;
(2)根据反应物的状态和反应条件选择发生装置,用无水醋酸钠固体与碱石灰固体在加热的条件下制取CH4,属固固加热型,故还需要试管。