题目内容
【题目】人类的生产生活离不开水。
(1)下列净化水的措施中,相对净化程度较高的是_____(填字母)。
A 静置沉淀 B 吸附沉淀 C 过滤 D 蒸馏
(2)与漫灌相比,喷灌和滴灌的优点是_____。
(3)含有较多可溶性钙、镁化合物的水叫做硬水,检验生活用水是硬水还是软水常用的试剂为_____。
(4)过滤是实验室分离可溶物和不溶物常用的操作。过滤时用到的玻璃仪器有下列选项中的_____。
A 烧杯 B 玻璃棒 C 铁架台 D 漏斗
(5)铁丝燃烧时盛有氧气的集气瓶底部需放少量水,是因为_____。
(6)净水器中常用到活性炭,这是利用了活性炭的_____性。
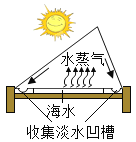
(7)海水淡化可缓解淡水资源匮乏的问题。下图为太阳能海水淡化装置示意图。海水制备淡水的过程属于_____(填“物理”或“化学”)变化。
【答案】D 节约用水 肥皂水 ABD 防止集气瓶炸裂 吸附(吸附性) 物理
【解析】
(1)净化水的单一操作中,蒸馏可以除去水中的所有杂质,因此相对净化程度较高的是蒸馏,故选:D;
(2)与漫灌相比,喷灌和滴灌的优点是节约用水;故填:节约用水;
(3)硬水和软水的区别在于所含的钙镁离子的多少,生活中可用肥皂水来区分硬水和软水,产生泡沫较多的是软水,较少的硬水;故填:肥皂水;
(4)过滤时用到的玻璃仪器有烧杯、漏斗、玻璃棒;故填:ABD;
(5)铁丝燃烧时盛有氧气的集气瓶底部需放少量水,这是为了防止高温生成物溅落、炸裂瓶底;故填:防止集气瓶炸裂;
(6)活性炭具有吸附性,可以除去水中的色素和异味;故填:吸附;
(7)海水制备淡水的过程中没有新物质生成,发生的属于物理变化;故填:物理。

【题目】(1)矿物质水中元素及国标含量如下表所示,请用化学用语回答下列问题。
矿物质水中主要成分(mg/L) | |
偏硅酸 硫酸根 氯离子 | 钙 钠 钾 镁 |
①矿物质水中含有的镁元素_____;
②久置的水中溶有一定量的氧气,请表示出2个氧分子_____;
③表中的一种阴离子_____;
(2)现有H、O、N、C四种元素,请选用其中的元素写出符合下列要求的物质各一个(用化学式表示):
①焊接金属时常用作保护气的是_____﹔②人体中含量最多的物质_____;③供给呼吸的气体是_____。
【题目】(1)英国科学家法拉第曾以蜡烛为主题,对青少年发表了一系列演讲,其演讲内容被编成《蜡烛的化学史》一书。下列有关蜡烛燃烧的叙述正确的是(________)
A 蜡烛燃烧时,在顶端会形成一个液态石蜡的凹槽
B 用玻璃管从蜡烛火焰中引出的白烟是水蒸气
C 蜡烛燃烧时,液态石蜡抵达烛芯上汽化并燃烧
(2)“分解过氧化氢制氧气的反应中二氧化锰的催化作用”,以及“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣。
[提出问题]氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
[实验探究]
实验步骤 | 实验现象 |
I.分别量取5 ml 5%过氧化氢溶液放入A、B两支试管中,向A试管中加入a g氧化铁粉末,并分别在A、B两支试管中插入带火星木条,观察现象。 | A试管中产生气泡,带火星木条复燃,B试管中无明显现象 |
II.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,试管中均产生气泡,带火星木条均复燃如此反复多次试验,观察现象。 | 式管中均产生气泡,带火星木条均复燃 |
III.将实验II中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为a g。 | / |
IV.分别量取5 ml 5%过氧化氢溶液放入C、D两支试管中,向C试管中加入a g氧化铁粉末,向D试管中加入a g二氧化锰粉末,观察现象。 | / |
[实验结论]
①A中产生的气体是_____。
②实验II、III证明:氧化铁的_____和_____在反应前后均没有发生变化,可以作过氧化氢分解的催化剂。
[实验评价]
③实验设计IV的目的是_____。
(3)10 g A和足量B混合加热,充分反应后10 g A生成6 g C和8 g D,则参加反应的A和B的质量比为(________)
A 1∶1 B 2∶3 C 4∶1 D 5∶2