题目内容
已知金属钠和水能发生下列反应:2Na+2H2O═2NaOH+H2↑,现将一定质量的金属钠放入75.6克水中,反应后生成8克氢氧化钠,计算:
(1)参加反应的水是多少克?
(2)反应后得到的氢氧化钠溶液中溶质的质量分数是多少?
(1)参加反应的水是多少克?
(2)反应后得到的氢氧化钠溶液中溶质的质量分数是多少?
分析:(1)根据钠和水反应的化学方程式,通过生成氢氧化钠的质量可以计算出参加反应的水的质量;
(2)计算氢氧化钠溶液的质量分数时,溶液的质量是水的质量与加入的钠的质量和减去生成氢气的质量,可以据此完成解答.
(2)计算氢氧化钠溶液的质量分数时,溶液的质量是水的质量与加入的钠的质量和减去生成氢气的质量,可以据此完成解答.
解答:解:(1)设参加反应的水的质量为x,生成氢气的质量为y,参加反应的钠的质量为z,则
2Na+2H2O═2NaOH+H2↑
46 36 80 2
z x 8g y
=
=
=
解之得:x=3.6g,y=0.2g,z=4.6g.
(2)反应后得到的氢氧化钠溶液中溶质的质量分数=
×100%=10%;
答:(1)参加反应的水是3.6克;
(2)反应后得到的氢氧化钠溶液中溶质的质量分数10%.
2Na+2H2O═2NaOH+H2↑
46 36 80 2
z x 8g y
| 36 |
| x |
| 2 |
| y |
| 46 |
| z |
| 80 |
| 8g |
解之得:x=3.6g,y=0.2g,z=4.6g.
(2)反应后得到的氢氧化钠溶液中溶质的质量分数=
| 8g |
| 4.6g+75.6g-0.2g |
答:(1)参加反应的水是3.6克;
(2)反应后得到的氢氧化钠溶液中溶质的质量分数10%.
点评:本题主要考查学生根据化学方程式找出已知量和未知量的关系列比例式求解问题的能力及溶质质量分数的计算问题.根据化学方程式的计算,就是依据反应物和生成物间的质量比进行的;已知反应物的质量可以算出生成物的质量,反之,已知生成物的质量也可以算出所需反应物的质量.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
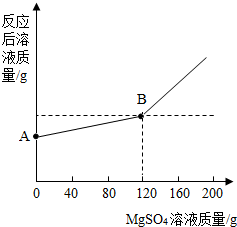 已知金属钠和水能发生下列反应:2Na+2H2O=2NaOH+H2↑
已知金属钠和水能发生下列反应:2Na+2H2O=2NaOH+H2↑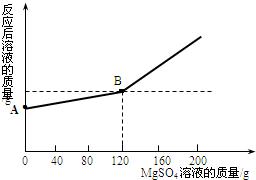 20、已知金属钠和水能发生反应:2Na+2H2O=2NaOH+H2↑
20、已知金属钠和水能发生反应:2Na+2H2O=2NaOH+H2↑