题目内容
相同质量的CO2和SO2中,含氧量之比为分析:物质质量相同,求物质的含氧量之比时,将物质质量看作“1”,然后表示出每种物质中氧元素的质量,最后再相比即可;
物质的含氧量相同,求物质的质量比时,将物质中氧元素的质量看作“1”,然后表示出每种物质的质量,最后再相比即可.
物质的含氧量相同,求物质的质量比时,将物质中氧元素的质量看作“1”,然后表示出每种物质的质量,最后再相比即可.
解答:解:相同质量的二氧化碳和二氧化硫中含氧量之比为
1×
:1×
=16:11
二氧化碳和二氧化硫中含氧量相同时两物质的质量比为
:
=11:16
故答案为:16:11,11:16.
1×
| 16×2 |
| 44 |
| 16×2 |
| 64 |
二氧化碳和二氧化硫中含氧量相同时两物质的质量比为
| 1 | ||
|
| 1 | ||
|
故答案为:16:11,11:16.
点评:本题主要考查有关化学式的计算,难度较大.关键是对“物质中某元素的质量分数”的计算公式地灵活运用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
某学习小组对用碳酸盐可以制取CO2进行如下研究:

(1)向盛有等质量块状纯碱固体和块状碳酸钙固体的两装置中同时分别加入足量的相同质量相同浓度的稀盐酸,测得生成的CO2质量与时间关系如下表.
①从表中数据获得信息______.
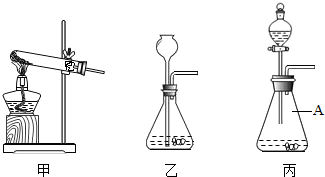
②如图是一组实验装置,该实验除用到电子秤外,还需用图中______装置(填所选装置编号).
③实验中小红同学用沾有紫色石蕊试液的玻璃棒放在所选装 置的导管口检验生成的气体,观察到的现象为______,由此她认为产生的气体为CO2.小军同学认为小红同学的验证不严密,理由是______.
④请写出块状碳酸钙固体与稀盐酸反应方程式为______.
⑤由上表数据可知,若用块状纯碱晶体代替块状石灰石制取CO2,为保证实验时间接近,所用稀盐酸质量分数需______(选填“变大”、“变小”或“不变”).
(2)若需制取较纯净的CO2,则最好选择下列哪组药品?______,因为:______.
A.块状石灰石与稀盐酸 B.块状石灰石与稀硫酸
C.块状纯碱晶体与稀盐酸 D.块状纯碱晶体与稀硫酸
(3)丙图中标号仪器A的名称为______,用装置甲制取氧气的化学反应方程式为______ K2MnO4+MnO2+O2↑

(1)向盛有等质量块状纯碱固体和块状碳酸钙固体的两装置中同时分别加入足量的相同质量相同浓度的稀盐酸,测得生成的CO2质量与时间关系如下表.
| 生成CO2质量/g | 2 | 4 | 6 | 8 | 12 | |
| 时间/s | 块状碳酸钙固体 | 10 | 25 | 40 | 60 | 85 |
| 块状纯碱晶体 | 4 | 9 | 15 | 25 | 40 | |
②如图是一组实验装置,该实验除用到电子秤外,还需用图中______装置(填所选装置编号).
③实验中小红同学用沾有紫色石蕊试液的玻璃棒放在所选装 置的导管口检验生成的气体,观察到的现象为______,由此她认为产生的气体为CO2.小军同学认为小红同学的验证不严密,理由是______.
④请写出块状碳酸钙固体与稀盐酸反应方程式为______.
⑤由上表数据可知,若用块状纯碱晶体代替块状石灰石制取CO2,为保证实验时间接近,所用稀盐酸质量分数需______(选填“变大”、“变小”或“不变”).
(2)若需制取较纯净的CO2,则最好选择下列哪组药品?______,因为:______.
A.块状石灰石与稀盐酸 B.块状石灰石与稀硫酸
C.块状纯碱晶体与稀盐酸 D.块状纯碱晶体与稀硫酸
(3)丙图中标号仪器A的名称为______,用装置甲制取氧气的化学反应方程式为______ K2MnO4+MnO2+O2↑



 某学习小组对用碳酸盐可以制取CO2进行如下研究:
某学习小组对用碳酸盐可以制取CO2进行如下研究: