��Ŀ����
����Ŀ��ij��ѧС��ι��Ƽ�����˸ó���������Ĺ�������ͼ���£���ͼ�ش�
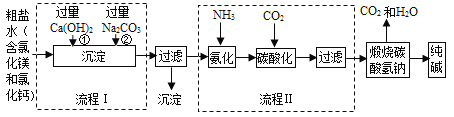
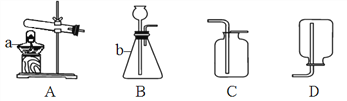
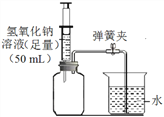
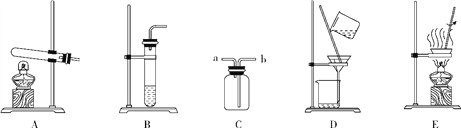
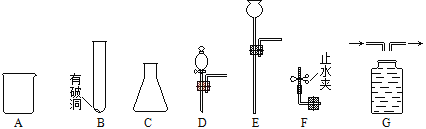
(1)����ͼ�������������ˮ�м���Ca(OH)2��Na2CO3���������˳���ܷ�ߵ���______(�����ܻ����)��Ϊʲô___________________��
(2)����I�õ��ij����ɷ��У�______________��______________(�ѧʽ)
(3)��������Ȼ����ΪĿ���Ʒ�������백������Ϊ���������Ȼ�泥���ô���������Ƽ�����е�����_______________________��
(4)���̢����ķ�Ӧ����ʽΪ��___________________________
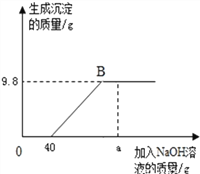
(5)20��ʱ����100gˮ�м���11.7g�Ȼ��ƺ�15.8g̼����泥���ַ�Ӧ�������ϴ���Һ���������������Ϊ_______g ��(20��ʱ̼�����Ƶ��ܽ��Ϊ9.7g���Ȼ�淋��ܽ��Ϊ37.2g)
���𰸡� ���ܵߵ��� ����ߵ����������������ƺ������ɵ��Ȼ�������ȥ Mg(OH)2 CaCO3 ʹ��Һ�Լ��ԣ����������̼�������� NaCl+H2O+NH3+CO2==NaHCO3+NH4Cl 7.1g
��������(1)���������ˮ�м���Ca(OH)2��Na2CO3��˳���ܵߵ�������ߵ����������������ƺ������ɵ��Ȼ��ƽ�����ȥ��(2)MgCl2 + Ca(OH)2 ==Mg(OH)2��+ CaCl2��Na2CO3 + Ca(OH)2 == CaCO3��+ 2NaOH��Na2CO3 + CaCl2 == CaCO3��+ 2NaCl�����Թ���I�õ��ij����ɷ���Mg(OH)2��CaCO3(3)����������ˮ�γɰ�ˮ����ˮ���ڼʹ��Һ������ǿ�����������̼����������(4)���ݻ�ѧ��Ӧǰ��Ԫ�ص�����䣬���̢����ķ�Ӧ����ʽΪ��NaCl+H2O+NH3+CO2==NaHCO3+NH4Cl (5)20��ʱ��NaCl���ܽ����36g������100gˮ������ܽ�36gNaCl����100gˮ�м���11.7g�Ȼ��ƣ������������壻NaCl+NH4HCO3==NaHCO3+NH4Cl�����ݻ�ѧ���̼����֪��11.7g�Ȼ��ƺ�15.8g̼�����ǡ�÷�Ӧ��������NaHCO3������Ϊx��NH4Cl������Ϊy
NaCl+NH4HCO3==NaHCO3+NH4Cl
79 84 53.5
15.8g x y
![]() =
=![]() �����x=16.8g��
�����x=16.8g�� ![]() =
=![]() �����y=10.7g
�����y=10.7g
20��ʱ�Ȼ�淋��ܽ��Ϊ37.2g�������Ȼ��������20��ʱ̼�����Ƶ��ܽ��Ϊ9.7g����������̼�����Ƶ������ǣ�16.8g-9.7g=7.1g