题目内容
【题目】有一包白色固体样品,可能由氢氧化钠、碳酸钙、氯化钡、氯化镁、硫酸钠5种物质中的几种组成。为探究样品的组成,某小组取适量样品按下图所示流程进行实验。请结合图中信息。回答相关问题。
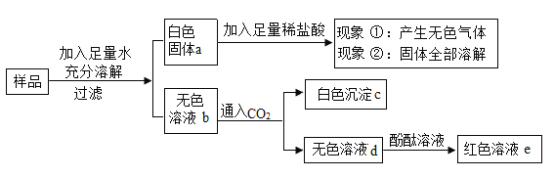
(1)白色固体a中一定含有的物质是_____。
(2)写出现象①对应的化学反应方程式_____。
(3)无色溶液b中含有的溶质成分是_____。
(4)关于上述实验过程的分析,下列说法中正确的是_____。
A原固体样品中一定不含硫酸钠
B白色固体a和白色固体c的成分可能相同
C白色固体c中滴加稀硫酸沉淀全部溶解
D向红色溶液e中加入氯化钡溶液即可确定其成分
【答案】CaCO3(或碳酸钙) ![]() NaOH和BaCl2(或一定含有NaOH、BaCl2,可能含有NaCl) A
NaOH和BaCl2(或一定含有NaOH、BaCl2,可能含有NaCl) A
【解析】
(1)向样品中加入足量的水溶解后得到不溶性固体a,根据题目中几种可能存在的物质的性质可知:不溶于水的碳酸钙可能存在,白色固体a中还有可能含有氢氧化钠与氯化镁反应生成的氢氧化镁以及硫酸钠与氯化钡反应生成的硫酸钡,再向a中加入足量的稀盐酸后生成无色气体,证明a中含有碳酸钙,加入稀盐酸后固体a全部溶解,证明固体a中不含硫酸钡,上述实验并不能证明a中是否含有氢氧化镁,所以白色固体a中一定含有的物质是碳酸钙,故填CaCO3(或碳酸钙)。
(2)由(1)可知,现象①对应的化学反应是碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,故反应的化学方程式写为:CaCO3+2HCl=CaCl2+H2O+CO2↑。
(3)由(1)可知,无色溶液b中一定不含碳酸钙,向无色溶液b中通入二氧化碳后生成白色固体c,二氧化碳与氢氧化钠反应生成碳酸钠和水,碳酸钠与氯化钡反应生成碳酸钡沉淀和氯化钠,所以无色溶液b中含有的溶质成分应该是氢氧化钠和氯化钡,由(1)又知,白色固体a中还有可能含有氢氧化钠与氯化镁反应生成的氢氧化镁,氢氧化钠与氯化镁反应除生成氢氧化镁外还生成氯化钠,所以无色溶液b中还可能含有氯化钠,故填NaOH和BaCl2(或一定含有NaOH、BaCl2,可能含有NaCl)。
(4)A 由(1)可知,白色固体a中不含硫酸钡,则原样品中最多含有氯化钡与硫酸钠中的一种,由(3)可知,原样品中一定含有氯化钡,所以原固体样品中一定不含硫酸钠,选项正确;
B 由(1)可知,白色固体a中含有碳酸钙,原样品中除碳酸钙中含有钙元素外,其它物质不含钙元素,所以无色溶液b中通入二氧化碳后不可能生成碳酸钙,即白色固体a和白色固体c的成分一定不相同,选项错误;
C 白色固体c是碳酸钡,碳酸钡与稀硫酸反应生成硫酸钡沉淀、水和二氧化碳,沉淀并没有完全消失,选项错误;
D 由(3)可知,无色溶液b中一定含有氢氧化钠与氯化钡,向其中通入二氧化碳后,氢氧化钠与二氧化碳反应后可能有剩余,氢氧化钠与二氧化碳反应生成的碳酸钠与氯化钡反应时也有可能剩余,所以得到的红色溶液e中可能含有氢氧化钠与碳酸钠两种物质,加入的氯化钡溶液只与碳酸钠反应生成白色沉淀碳酸钡证明碳酸钠存在,但不能验证氢氧化钠是否存在,选项错误,故填A。