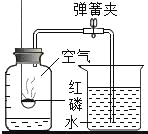
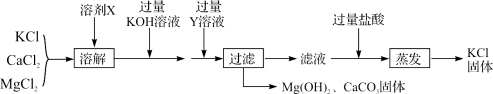
题目内容
【题目】请依据下列信息回答有关问题:
Cl2是一种黄绿色、具有刺激性气味、有毒的气体,其密度比空气的密度大.能与氢氧化钠溶液反应,生成氯化钠、次氯酸钠(NaClO)和水.Cl2可用于漂白纸张、布匹以及消毒饮用水等.在实验室里常用下述反应制取氯气:MnO2+4HCl(浓)![]() MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
(1)写出氯气与氢氧化钠溶液反应的化学方程式:______;生成物中氯元素的化合价分别为______.
(2)实验室选择气体发生装置应考虑的因素有哪些?______
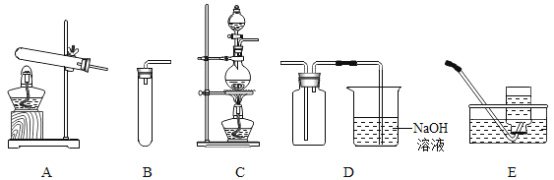
(3)如图,在实验室里制取氯气应选择的发生装置是______(填字母);收集氯气选用D装置,请推测其中氢氧化钠溶液的作用是______.
(4)如图,若选用B、E组合在实验室可制取气体,反应方程式为______.
(5)12.5g大理石与稀盐酸完全反应后,可生成二氧化碳气体4.4g,请计算大理石中杂质的质量分数______.
【答案】Cl2+2NaOH═NaCl+NaClO+H2O ﹣1、+1 反应物的状态和反应的条件 C 吸收多余的氯气 氧气;2H2O2![]() 2H2O+O2↑;(或氢气;Zn+H2SO4═ZnSO4+H2↑) 20%
2H2O+O2↑;(或氢气;Zn+H2SO4═ZnSO4+H2↑) 20%
【解析】
(1)根据氯气与氢氧化钠溶液反应原理书写方程式,并依据化合物中正负化合价总和为0的原则解答;
(2)根据实验室制取气体的一般思路:选择发生装置时要考虑反应物的状态和反应条件进行回答;
(3)根据反应物的状态和反应条件选择制取氯气的发生装置,氯气有毒,所以要进行尾气处理,并依据氯气可与氢氧化钠溶液反应分析解答;
(4)B、E组合在实验室可制取用固体和液体不需加热制取、且不易溶于水的气体,再根据反应原理书写方程式;
(5)根据大理石与稀盐酸反应方程式,依据二氧化碳气体的质量计算碳酸钙的质量,并进而求出大理石中杂质的质量分数。
(1)氯气能与氢氧化钠溶液反应,生成氯化钠、次氯酸钠(NaClO)和水,方程式是![]() ,氯化钠中钠元素显+1价,所以氯元素显﹣1价,次氯酸钠中钠元素显+1价,氧元素显﹣2价,所以氯元素显+1价;故答案为:
,氯化钠中钠元素显+1价,所以氯元素显﹣1价,次氯酸钠中钠元素显+1价,氧元素显﹣2价,所以氯元素显+1价;故答案为:![]() ;-1、+1;
;-1、+1;
(2)此题考查实验室制取气体的思路,选择发生装置时要考虑反应物的状态和反应条件;故答案为:反应物的状态和反应的条件;
(3)根据(2)中分析选择发生装置要考虑反应物的状态和反应条件,因实验室制取氯气是用加热二氧化锰和浓盐酸的方法,即反应物为固体和液体,反应的条件为加热,所以应选C装置,由于氯气有毒,并能与氢氧化钠反应,故可用氢氧化钠溶液吸收多余的氯气;
故答案为:C;吸收多余的氯气;
(4)B、E组合在实验室可制取用固体和液体不需加热制取、且不易溶于水的气体,实验室用双氧水制取氧气及用锌与稀硫酸反应制取氢气符合条件,氢气和氧气都不溶于水,双氧水和二氧化锰混合生成水和氧气,方程式是 ,锌与稀硫酸反应生成硫酸锌,方程式是
,锌与稀硫酸反应生成硫酸锌,方程式是![]() ;
;
故答案为:氧气, ;(或氢气,
;(或氢气,![]() )
)
(5)设CaCO3 的质量为x.

![]()
x=10g
大理石中杂质的质量分数为=![]()
故答案:
(1)![]() ;﹣1、+1
;﹣1、+1
(2)反应物的状态和反应的条件.
(3)C;吸收多余的氯气;
(4)氧气, (或氢气,
(或氢气,![]() );
);
(5)大理石中杂质的质量分数为20%。

【题目】下表是空气中的气体成分和人体呼出的气体成分含量对照表:
气体成分 | 氮气 | 氧气 | 二氧 化碳 | 水 | 其他 气体 |
空气中的气体/% | 78 | 21 | 0.03 | 0.07 | 0.9 |
呼出的气体/% | 78 | 16 | 4 | 1.1 | 0.9 |
某校研究性学习小组的同学设计了简单的实验方案,验证呼出的气体与吸入空气成分的含量的不同,其主要操作步骤如下图所示。
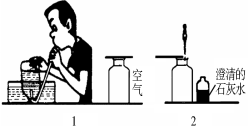
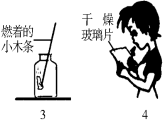
请依据图示将主要实验操作步骤及验证依据填入下表中:
实验步骤 | 验证依据 |
(1)___________________________________ | — |
(2)___________________________________ | 根据________________________判断CO2含量不同 |
(3)___________________________________ | 根据________________________判断O2含量不同 |
(4)___________________________________ | 根据________________________判断含水量不同 |
【题目】某化学兴趣小组的同学在学习九年级《化学》下册中的资料卡片“石笋和钟乳石的形成”时,发现难溶于水的碳酸钙当遇到溶有二氧化碳的水时,会反应生成溶解性较大的碳酸氢钙:CaCO3+CO2+H2O=Ca(HCO3)2,联想到实验室中澄清石灰水与二氧化碳反应会生成碳酸钙:Ca(OH)2+CO2=CaCO3↓+H2O,对长时间向碱溶液中通入CO2反应后溶液中的溶质组成产生了浓度的兴趣。
(提出问题)一定量CO2与NaOH溶液反应后的溶质组成是什么?
(查阅资料)(1)通入少量CO2反应的化学方程式为:_____。
(2)通入过量CO2,反应的化学方程式为:Na2CO3+CO2+H2O=2NaHCO3。
(3)碳酸氢盐都是可溶于水的,BaCO3难溶于水。
(4)碳酸氢钠溶液呈碱性。
(提出猜想)(1)溶质为NaOH和Na2CO3;
(2)溶质为Na2CO3;
(3)溶质为_____(填化学式);
(4)溶质为NaHCO3。
(设计实验)
实验步骤 | 实验现象 | 实验结论 |
(1)用玻璃棒蘸取反应后溶液,滴在pH试纸上 | pH=9 | 该溶液显碱性 |
(2)取反应后溶液少许于试管中,向其中滴加过量的BaCl2溶液 | 有_____生成 | 猜想(4)不成立 |
(3)取步骤(2)中的上层清液,滴入稀盐酸 | 有气泡冒出 | 猜想(1)和(2)不成立 |
(得出结论)猜想(3)成立。
(讨论交流)(1)有同学提出,实验步骤(1)是多余的。你认为该实验设计是否需要?_____(填“需要”或“不需要”)。
(2)同学们又一次把目光投向了教材,发现遇热或压强变小时:Ca(HCO3)2=CaCO3↓+CO2↑+H2O,纷纷提出,干粉灭火器中用NaHCO3灭火的反应原理与之相似,试写出NaHCO3受热分解的化学方程式_____。
(反思应用)同学们回忆起实验室检验二氧化碳的情景,心想:如果向澄清石灰水中不断通入二氧化碳,会看到怎样的现象呢?请你描述一下:_____。