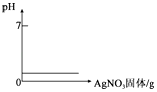题目内容
【题目】下列图象不能正确反映对应变化关系的是( )
|
|
|
|
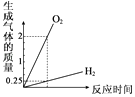
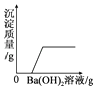
A、将水通电电解一段时间 | B、向稀盐酸中加入AgNO3固体 | C、等质量的铁粉和锌粉中分别加入足量的溶质质量分数相同的稀硫酸 | D、向H2SO4和MgCl2的混合溶液中逐滴加入Ba(OH)2溶液至过量 |
A.A
B.B
C.C
D.D
【答案】D
【解析】解:A、电解水生成氢气和氧气,反应的化学方程式及其质量关系为:
2H2O | 2H2↑+ | O2↑, |
36 | 4 | 32 |
由质量关系可知,生成氢气和氧气的质量比为:0.25:2=1:8=4:32,该选项对应关系正确;
B、稀盐酸和硝酸银反应生成氯化银沉淀和硝酸,随着反应的进行,消耗盐酸的同时生锈硝酸,溶液酸性不变,该选项对应关系正确;
C、铁和稀硫酸反应生成硫酸亚铁和氢气,锌和稀硫酸反应生成硫酸锌和氢气,等质量的铁粉和锌粉中分别加入足量的溶质质量分数相同的稀硫酸,随着硫酸的消耗,生成氢气质量开始一段时间相等,最终铁和稀硫酸反应生成的氢气多,该选项对应关系正确;
D、向H2SO4和MgCl2的混合溶液中逐滴加入Ba(OH)2溶液时,氢氧化钡能和硫酸反应生成硫酸钡沉淀和水,能和氯化镁反应生成氢氧化镁沉淀和氯化钡,向H2SO4和MgCl2的混合溶液中逐滴加入Ba(OH)2溶液至过量,一开始就反应生成沉淀,该选项对应关系不正确.
故选:D.
【考点精析】根据题目的已知条件,利用电解水实验和金属材料的选择依据的相关知识可以得到问题的答案,需要掌握电解水的实验:A.装置―――水电解器B.电源种类---直流电C.加入硫酸或氢氧化钠的目的----增强水的导电性D.化学反应:2H2O=== 2H2↑+ O2↑;黑色金属:通常指铁、锰、铬及它们的合金.重金属:如铜、锌、铅等;有色金属轻金属:如钠、镁、铝等;有色金属:通常是指除黑色金属以外的其他金属.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案