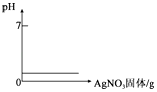题目内容
【题目】如图是胃得乐牌胃药的部分标识.胃药中所含的物质能中和胃里过多的胃酸(胃液质量约100g,主要是成分为盐酸).某患者按标识上的服用方法服药后病情好转.
试计算:
(1)患者在一次所服用的此胃药中,所含氢氧化镁的质量为 g.
(2)理论上可中和胃酸中的HCl的质量分数为多少?(最终计算结果保留0.1%)
【答案】
(1)0.5
(2)
解:设可中和胃酸中的HCl的质量为x
Mg(OH)2+ | 2HCl═MgCl2+2H2O |
58 | 73 |
0.5g | x |
∴ ![]()
解之得:x≈0.63g
理论上可中和胃酸中的HCl的质量分数为 ![]() =0.6%
=0.6%
【解析】解:(1)250mg×2=500mg=0.5g;
【考点精析】认真审题,首先需要了解根据化学反应方程式的计算(各物质间质量比=系数×相对分子质量之比).

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】在一密闭容器中有甲、乙、丙、丁四种物质,一定条件下使之反应,一段时间后测得反应前后各物质的质量如表:
物质 | 甲 | 乙 | 丙 | 丁 |
反应前质量/g | 90 | 9 | 0 | 2 |
反应后质量/g | 22 | 45 | 32 | X |
(1)此反应的基本反应类型;
(2)X的值 , 则丁可能是该反应的 .
(3)写出一个符合上述反应类型的化学方程式.
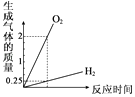
【题目】下列图象不能正确反映对应变化关系的是( )
|
|
|
|
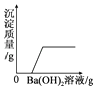
A、将水通电电解一段时间 | B、向稀盐酸中加入AgNO3固体 | C、等质量的铁粉和锌粉中分别加入足量的溶质质量分数相同的稀硫酸 | D、向H2SO4和MgCl2的混合溶液中逐滴加入Ba(OH)2溶液至过量 |
A.A
B.B
C.C
D.D