题目内容
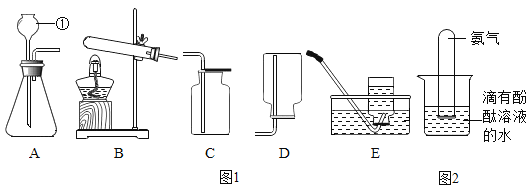
【题目】如图1中A~F为常见实验装置,请根据要求填空。
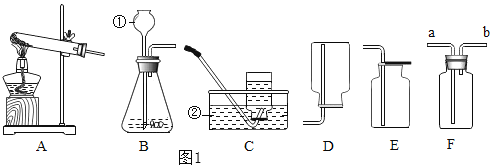
(1)写出标号仪器的名称:①__________ ; ②__________。
(2)实验室用高锰酸钾制取氧气,反应的化学方程式为____________,应选用的发生装置是__________(填字母,下同),以高锰酸钾为试剂利用此装置制取氧气时,还要做的改进是________________。用E装置收集氧气,检验氧气是否集满的方法_____________。小明同学想用装置F收集一瓶氧气,气体从_______端通入。
(3)小李同学想用过氧化氢溶液和二氧化锰混合制取较纯净的氧气,他应选用的装置组合是图1中的__________。实验时,可将①替换成________________,其优点是____________________。
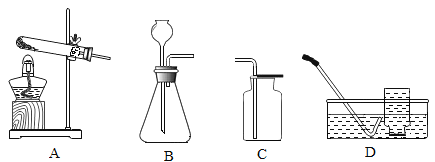
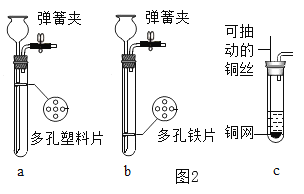
(4)实验室制备CO2时,要求能随时控制反应进行或停止,图2的发生装置正确且符合要求的是__________(选填字母)。
【答案】长颈漏斗 水槽 2KMnO4![]() K2MnO4+ MnO2+O2↑ A 在试管口塞一团棉花 将带火星的木条放在集气瓶口,若木条复燃,证明O2已满 a BC 分液漏斗 可以控制反应速率 c
K2MnO4+ MnO2+O2↑ A 在试管口塞一团棉花 将带火星的木条放在集气瓶口,若木条复燃,证明O2已满 a BC 分液漏斗 可以控制反应速率 c
【解析】
(1)①为加入液体的长颈漏斗,②为盛取液体的水槽;
故答案为:长颈漏斗;水槽。
(2)高锰酸钾在加热条件下分解生成锰酸钾、二氧化锰和氧气,据此书写化学方程式;反应物为固体,反应条件为加热,所以选择A;高锰酸钾为粉末固体,防止其被气体带入导管,应在试管口增加一小团棉花;氧气可使带火星的木条复燃,因此可以将带火星的木条置于瓶口,观察木条是否复燃,判断是否集满;万能瓶收集氧气时,氧气密度大于空气,先在底部聚集,所以氧气从长口a进入,将空气从短口b排出,达到收集气体的目的;
故答案为:2KMnO4![]() K2MnO4+MnO2+O2↑;A;在试管口塞一团棉花;将带火星的木条放在集气瓶口,若木条复燃,证明O2已满;a。
K2MnO4+MnO2+O2↑;A;在试管口塞一团棉花;将带火星的木条放在集气瓶口,若木条复燃,证明O2已满;a。
(3)过氧化氢溶液和二氧化锰为固液混合物,反应不需要加热,所以选择B作为发生装置,收集较为纯净的氧气,避免空气混入,选择排水法收集,所以选择C收集气体;长颈漏斗不具有活塞,加入液体为一次性加入,无法控制反应物的量,换为分液漏斗后,借助分液漏斗的活塞,控制加入过氧化氢溶液的量来控制反应速率;
故答案为:BC;分液漏斗;可以控制反应速率。
(4)a、多孔塑料板位置过高,收集气体的的量较少,不足以产生足够大的压强将液体压入长颈漏斗,无法实现固液分离,反应不能做到及时的发生与停止,a错误;
b、实验室用大理石和稀盐酸反应制取二氧化碳,多孔铁片会与稀盐酸反应生成氢气,使收集的二氧化碳不纯,且铁片被消耗,不能实现固液分离,b不可以控制反应的发生与停止,b错误;
c、利用可抽到的铜丝,将铜网内盛有的固体拉高,实现固液分离,反应停止,而再将铜丝向下移动,铜网内的固体与液体再接触,反应开始,所以c可以控制反应的发生与停止,c正确;
故答案为:c。

 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案【题目】硫酸铜晶体常用于杀虫、杀菌,用废铜料(含少量铁)生产硫酸铜晶体的流程如图所示,请回答下列问题.
![]()
(1)操作 a 的名称是_____;
(2)废铜料中加入足量试剂 X 的目的是_____;
(3)黑色固体 B 与试剂 X 的反应化学方程式是______;
(4)盛放硫酸铜溶液不宜用铁制容器的原因是(用化学方程式解释)______;
(5)根据硫酸铜的溶解度表格所示,最后硫酸铜溶液可以通过蒸发浓缩、_____,过滤、洗涤、干燥的方法得到硫酸铜晶体。
0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 60℃ | 80℃ | 100℃ | |
硫酸铜/g | 23.1 | 27.5 | 32 | 37.8 | 44.6 | 61.8 | 83.8 | 114 |