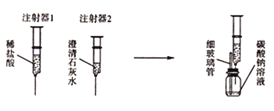题目内容
【题目】下列有关二氧化碳的说法正确的是
A.二氧化碳是引发酸雨的“罪魁” B.二氧化碳可使紫色石蕊试液变蓝
C.二氧化碳固体可用于人工降雨 D.二氧化碳有毒不能制作碳酸饮料
【答案】C
【解析】
试题分析:二氧化硫是引起酸雨的主要原因,A错误;二氧化碳易于水反应生成碳酸,碳酸能使紫色的石蕊试液变红,B错误;干冰升华时要吸收大量的热,能用于人工降雨,C正确;二氧化碳没有毒,能用于制做碳酸饮料,D错误。故选C。

 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案【题目】某金属单质 X与非金属单质Y可发生反应:2X+Y=X2Y.某实验探究小组进行了两次实验,测得数据如下表:
实验序号 | X的用量/g | Y的用量/g | 生成X2Y的质量/g |
1 | 7.4 | 1.6 | 8.0 |
2 | 9.6 | 3.2 | 12.0 |
参加反应的X与Y的质量比为
A.4:1 B.3:1 C.2:1 D.37:8
【题目】在学习酸、碱、盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的探究。

探究一:M溶液中的溶质是什么?
(1)【提出猜想】该组同学认为M溶液的溶质有两种可能:
①是 ,②是CaCl2。
【收集资料】CaCl2水溶液呈中性.
(2)【设计实验】同学们设计了如下方案并进行实验:
实验操作 | 实验现象 | 实验结论 |
取少量M溶液于试管中,向其中滴入 | 溶液变红 | 猜想①正确 |
探究二:过滤后澄清滤液中会有哪些溶质?
【提出猜想】
猜想一:NaOH和Na2CO3;
猜想二: ;
猜想三:NaOH.
(3)【实验验证】同学们针对“猜想一”进行如下实验:
实验操作 | 实验现象 | 实验结论 |
取样于试管中,滴入几滴稀盐酸 | 没有气泡产生 | “猜想一”不成立 |
他们的实验结论是否正确? (填“是”或“否”)
(4)【继续探究】设计如下实验方案确定滤液中溶质的组成.
实验操作 | 实验现象 | 实验结论 |
分别取少量滤液于A、B两支试管中,A中加入CaCl2溶液,B中加入 溶液 | 若A中产生白色沉淀,B中没有沉淀 | “猜想一”成立 |
“猜想二”成立 | ||
若A、B中都没有沉淀产生 | “猜想三”成立 |
(5)【反思与拓展】
①为防止标签被腐蚀而破损,倾倒液体时 。
②在分析反应后所得溶液中溶质时,除考虑可溶性的生成物,还应考虑 。