题目内容
【题目】以饱和 NaCl 溶液和饱和 NH4HCO3 溶液为原料制备
NaHCO3 的原理为:
NaCl+NH4HCO3=NaHCO3↓+NH4Cl
已知:碳酸氢铵在 40℃受热易分解。
回答下列问题:
(1)该反应中的四种物质溶解度曲线如图所示:
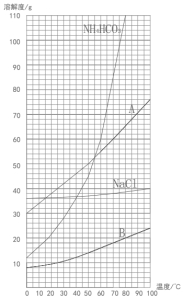
①35℃时,比较 A、B 溶解度的大小:A B。(填“>”或“<”)
②图中表示碳酸氢钠溶解度曲线的是 。(填“A”或“B”)
(2)为探究 NaHCO3 析出的最佳条件,完成了以下几组实验:
实验序号 | 反应温度/℃ | 反应时间/min | NaHCO3 产率/% |
a | 30 | 60 | 86.8 |
b | 30 | 120 | X |
c | 35 | 60 | 89.4 |
d | 35 | 120 | 92.5 |
e | 40 | 60 | 85.3 |
f | 40 | 120 | 85.6 |
①实验 c 和 d 的目的是 。
②表格中 X 的数值可能是 。
A.85.8 B.86.8 C.92.1 D.93.1
③在相同反应时间,40℃时碳酸氢钠的产率比 35℃时低的原因是 。
【答案】
(1)①> ②B
(2)①探究相同反应温度时,反应时间对 NaHCO3 产率的影响
②C
③在 40℃时 NH4HCO3 受热容易分解,导致反应物减少。
【解析】
试题分析:
(1)①观察图中 35℃时物质 A 的溶解度曲线在物质 B 上方,因此 A 的溶解度要大于 B。
②由题意可知,碳酸氢钠容易析出结晶形成沉淀,由图像可知溶解度 A>B,因此 B 为碳酸氢钠。
(2)①实验 c、d 的反应温度相同,而反应时间不同,因此是探究反应时间对产物产率的影响。
②由实验 a、c、e 可得:当反应时间相同,反应温度上升的过程中,产率是先上升再下降(下降是因为碳酸氢铵在 40℃时易分解)。因此实验 b、d、f 产率也应符合这一规律,因此 X 应大于 86.8 而小于 92.5。
③由题意可得,在 40℃时 NH4HCO3 受热容易分解,导致反应物减少。

 阅读快车系列答案
阅读快车系列答案