题目内容
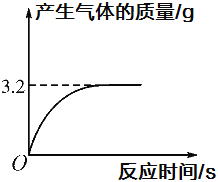
【题目】实验室有一瓶失去标签的过氧化氢溶液,为测定其溶质质量分数,兴趣小组同学取100g该溶液与1g二氧化锰混合,使其充分反应,产生气体的质量和反应时间关系如图。
(1)产生气体的速度越来越慢的原因是________,
A.二氧化锰越来越少
B.过氧化氢溶液的溶质质量分数越来越小
C.温度越来越高
(2)计算所用过氧化氢溶液的溶质质量分数。________(规范写出计算过程)
【答案】B 6.8%(详见解析)
【解析】
(1)根据影响反应进行的因素分析;
(2)根据生成气体的质量与反应时间的关系图,可得知所取过氧化氢完全反应放出氧气质量为3.2g,利用反应放出氧气的质量可计算所取溶液中过氧化氢的质量,则可计算该溶液中溶质的质量分数。
(1)A、二氧化锰作为催化剂反应前后质量和化学性质都不变,故A错误;B、反应物的浓度越小,反应速率越小,故B正确;C、温度越高,反应速率越大,故C错误。故选B;
(2)设:过氧化氢溶液中溶质的质量为x
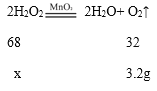
![]() x=6.8g
x=6.8g
该溶液中溶质的质量分数= ![]() =6.8%
=6.8%
答:该溶液中溶质的质量分数为6.8%。

 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案【题目】在一次化学兴趣小组活动中,老师拿来一瓶标签有破损的试剂瓶,如图,里面盛有一种无色溶液.该化学兴趣小组的同学对此展开探究:

(提出问题)这瓶无色溶液的溶质是什么呢?
(做出猜想)猜想一CaCO3;猜想二CaCl2;猜想三Ca(OH)2;猜想四Ca(NO3)2
(讨论交流)讨论后,大家一致认为猜想一是错误的,其理由是__________.
(查阅资料)CaCl2溶液、Ca(NO3)2溶液均是中性的.
(实验探究)为验证其余猜想,小组的四位同学分别设计了如下实验:
实验编号 | 实验一 | 实验二 | 实验三 | 实验四 |
实验方案 |
|
|
|
|
实验现象 | 产生白色沉淀 | 产生白色沉淀 | ||
实验结论 | 猜想三成立 | 猜想三成立 | 猜想三成立 | 猜想三成立 |
(得出结论)猜想三成立,此无色溶液为Ca(OH)2溶液.
(表达交流)(1)实验一的现象是___________.
(2)实验二的化学反应方程式为_______________.
(3)小组同学经过讨论,一至认为实验三不能证明猜想三成立,其理由是_____________.
(拓展迁移)(4)实验四中的X溶液可以选择__________(填字母序号)溶液.
(5)你认为取用化学试剂时为防止标签受损,倾倒液体时应__________.