题目内容
【题目】某化学兴趣小组的同学用粗盐(含有难溶性杂质可溶性杂质)做了如下实验:
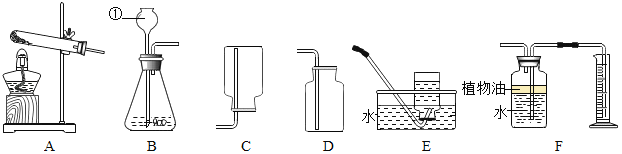
[实验一]:如图是同学们做粗盐提纯实验的操作示意图。请回答下列问题:

(1)下列说法正确的是_____(填选项字母)
A 此实验只能除去不溶性的杂质
B 称量粗盐是为了计算产率和计算量取水的体积
C 操作⑥时若滤纸没有紧贴漏斗内壁,则会影响过滤速度
D 蒸发时,蒸发皿应放在石棉网上加热
(2)操作④中用玻璃棒搅拌的作用是_____。
(3)粗盐提纯实验的操作顺序为(填序号)_____称量精盐并计算产率。产率偏低的可能原因是_____(填字母序号)
A 过滤时滤纸有破损
B 蒸发时液体有溅出
C 溶解含有泥沙的粗盐时,加入的水量过多
D 转移精盐时,蒸发皿中残留较多固体
[实验二]:为了除去粗盐中CaCl2、MgCl2、 Na2SO4 等可溶性杂质,需进行如下操作:①溶解:②依次加过量的BaCl2、NaOH、Na2CO3 溶液;③过滤;④加适量盐酸;⑤蒸发、结晶。
(4)以上操作中所发生的复分解反应共有_____个
(5)写出④操作中发生反应的化学方程式_____。
(6)请设计实验方案证明操作③所得溶液中含有NaOH。用量筒量取10mL③所得溶液倒入试管中,然后_____。(写出实验步骤即可)
【答案】ABC 防止由于局部温度过高造成液滴飞溅 ①⑤②③⑥④ BD 6 ![]() 、
、![]() 加入过量的硝酸钡溶液,过滤,向滤液中滴加无色酚酞溶液(合理即可)
加入过量的硝酸钡溶液,过滤,向滤液中滴加无色酚酞溶液(合理即可)
【解析】
(1)A 粗盐提纯实验只能除去不溶性的杂质,得到的晶体中还含有可溶性杂质,选项正确;
B 称量粗盐是为了计算产率和计算量取水的体积,选项正确;
C 操作⑥时若滤纸没有紧贴漏斗内壁,会造成浊液中的固体颗粒堵塞滤纸上的小孔,会影响过滤速度,选项正确;
D 蒸发时,蒸发皿可直接铁架台的铁圈或三脚架上加热,不需放在石棉网上加热,选项错误,故填ABC。
(2)操作④为蒸发,用玻璃棒搅拌的作用是防止由于局部温度过高造成液滴飞溅,故填防止由于局部温度过高造成液滴飞溅。
(3)粗盐提纯的实验步骤是取粗盐放到托盘天平上,称取一定质量的粗盐,将称量好的粗盐药品放入烧杯中,再量取一定体积的水倒入盛粗盐的烧杯中,用玻璃棒搅拌溶解,静置一段时间后过滤,最后将滤液蒸发得到食盐晶体,即该实验的实验步骤为①⑤②③⑥④,故填①⑤②③⑥④;
A 过滤时滤纸有破损会造成不溶性固体颗粒进入滤液,导致产率偏高,选项错误;
B 蒸发时液体有溅出造成蒸发后晶体质量偏小,导致产率偏低,选项正确;
C 溶解含有泥沙的粗盐时,加入的水量过多,不会造成实验的质量减少,不影响产率,选项错误;
D 转移精盐时,蒸发皿中残留较多固体,造成称量晶体的质量偏小,导致称量偏小,选项正确,故填BD。
(4)该操作中的化学反应有:氯化钡与硫酸钠反应生成硫酸钡沉淀和氯化钠、氢氧化钠与氯化镁反应生成氢氧化镁沉淀和氯化钠、碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠、碳酸钠与过量的氯化钡反应生成碳酸钡沉淀和氯化钠、稀盐酸与过量的氢氧化钠反应生成氯化钠与水和稀盐酸与过量碳酸钠反应生成氯化钠、水和二氧化碳共6个反应,且均属于复分解反应,故填6。
(5)④操作中加入的稀盐酸与过量的氢氧化钠反应生成氯化钠和水,反应的化学方程式为:NaOH+HCl=NaCl+H2O,稀盐酸与过量的碳酸钠反应生成氯化钠、水和二氧化碳,反应的化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑,故填NaOH+HCl=NaCl+H2O和Na2CO3+2HCl=2NaCl+H2O+CO2↑。
(6)操作③所得溶液中除含有过量的氢氧化钠,还有过量的碳酸钠,证明氢氧化钠存在的方法是加入过量的硝酸钡溶液除去碳酸钠,过滤,向滤液中滴加无色酚酞溶液,如果溶液呈红色,证明操作③所得溶液中除含有氢氧化钠,故填加入过量的硝酸钡溶液,过滤,向滤液中滴加无色酚酞溶液。

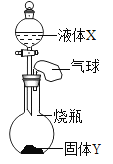
【题目】如图所示,将一定量的液体 X 滴入到烧瓶中,若小气球先鼓起,一段时间后又变瘪(液体 X的体积忽略不计),则液体 X 和固体 Y 是( )
选项 | 液体X | 固体Y |
A | 水 | 氧氧化钠 |
B | 水 | 碳酸铵 |
C | 过氧化氢溶液 | 二氧化锰 |
D | 稀盐酸 | 碳酸钠 |
A.AB.BC.CD.D