题目内容
【题目】水是由氢、氧两种元素组成的化合物。这一结论是科学家们在大量实险的基础上得出的。
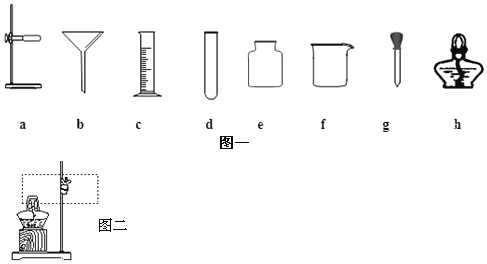
(1)实验室中常用锌粒和稀硫酸反应来制备氢气。请从下列装置中选择并组装一套制取较干燥氢气的装置,正确的连接顺序为______ (用接口处字母填写)。
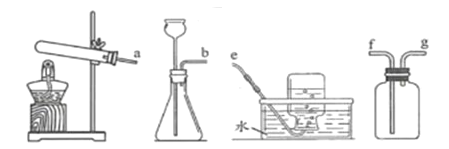
(2)研究氢气的燃烧实验是人们认识水组成的开始。氢气在点燃前一定要________。在相同条件下,欲使1L氢气完全燃烧,所需空气至少约为______L。
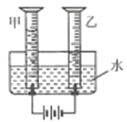
(3)科学家们又用“电解法”证明了水的组成(装置如图所示,电极不与水及生成的气体反应)。通电一段时间后,发现甲、乙两量简中收集的气体体积比略小于1:2,其原因可能是_________ (写出一条即可)。
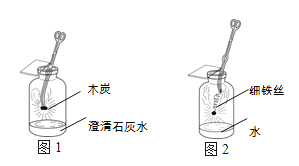
(4)用“氢气还原氧化铜”实验也可以证明水的组成。(碱石灰吸收反应生成的水)
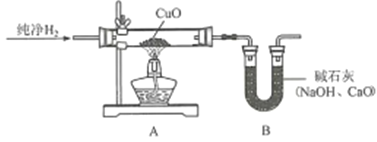
装置A中的玻璃管和其中物质在反应前后的质量差为m1,装置B和其中物质在反应前后的质量差为m2,据此可计算出水中O、H元素的质量比为______(用含m1、m2表示)
(5)拉瓦锡还用另一实验证明了水的组成。在高温条件下他让水蒸气通过一根烧红的铁质枪管,结果得到了氢气,同时枪管表面有黑色固体(磁铁矿的主要成分Fe3O4)生成。该反应的化学方程式为________。
【答案】b、g 或(b. g f ) 检验纯 度 2.5(或2.38) 在相同条件下,O2较H2稍易溶于水 ![]() 3Fe+4H2O
3Fe+4H2O![]() Fe3O4+4H2
Fe3O4+4H2
【解析】
(1)氢气是锌粒和稀硫酸反应是固体和液体混合不需要加热,氢气的密度小于空气的密度,用向下排空气法收集干燥氢气,所以连接顺序是:bgf;
(2)氢气具有可燃性,不纯点燃可能会发生爆炸,所以氢气在点燃前一定要验纯;氢气燃烧生成水,所以烧杯壁上有水雾;由方程式:2H2+O2![]() 2H2O可知1L氢气完全燃烧消耗0.5L氧气,因为氧气约占空气体积的
2H2O可知1L氢气完全燃烧消耗0.5L氧气,因为氧气约占空气体积的![]() (或21%),所以空气体积是2.5(或2.38)L;
(或21%),所以空气体积是2.5(或2.38)L;
(3)电解水加入氢氧化钠是为了增强水的导电性;甲、乙两量筒中收集的气体体积比略小于1:2,可能是氧气比氢气更易溶于水,或者部分氧气与电极发生了反应;
(4)装置A中的玻璃管和其中物质在反应前后的质量差为m1就是氧化铜中减少的氧元素的质量,也就是水中氧元素质量为m1;装置B和其中物质在反应前后的质量差为m2就是氢气与氧化铜反应生成的水的质量,即水的质量是:m2,所以水中氢元素质量为:m2-m1,所以O、H元素的质量比为m1:(m2-m1);
(5)反应物是铁和水,生成物是四氧化三铁和氢气,所以化学方程式为:3Fe+4H2O![]() Fe3O4+4H2↑。
Fe3O4+4H2↑。

 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案