题目内容
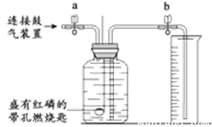
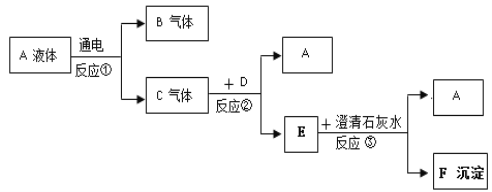
【题目】某校化学探究性学习小组的同学在学习了《金属与矿物》一章后,做了如下图所示的探究实验。实验发现CO与CuO加热后,黑色粉末变成红色粉末。请你参与该小组的探究过程并回答下列问题。
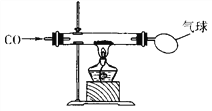
【探究课题】探究红色粉末的主要成分。
【查阅资料】
(1)有关物质的颜色:CuO粉末黑色,Cu2O粉末红色。
(2)CuO和Cu2O都能和稀硫酸发生反应,化学方程式:
CuO+H2SO4===CuSO4+H2O Cu2O+H2SO4===CuSO4+Cu+H2O
【猜想与实验】
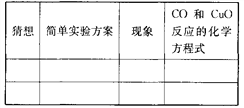
(1)如果硬质玻璃管内红色粉末为一种物质,请猜想它的成分,并设计简单的实验证明你的猜测。________________________________
(2)如果硬质玻璃管内红色粉末为两种物质的混合物,要确定粉末中两种物质的质量分数,还需要通过有关数据计算进行判断。下列数据不可作为计算依据的是 (______)
A.反应前CuO粉末的质量 B.硬质玻璃管中固体物质减少的质量
C.通入CO的质量 D.反应后固体混合物的总质量
【答案】
Cu | 取少年红色粉末,放于试管中,向其中加入稀盐酸 | 无明显现象 | CuO +CO |
Cu2O | 取少年红色粉末,放于试管中,向其中加入足量稀硫酸 | 溶液变为蓝色,仍有红色固体 | 2CuO +CO |
C
【解析】由题中信息可知,CuO和Cu2O都能和稀硫酸发生反应,化学方程式:CuO+H2SO4===CuSO4+H2O , Cu2O+H2SO4===CuSO4+Cu+H2O,而铜不能与硫酸反应,硫酸铜溶液为蓝色。设剩余固体只有铜,验证方案为:取少年红色粉末,放于试管中,向其中加入稀硫酸,无明显现象,可证明固体为铜,一氧化碳和氧化铜的反应方程式为:CuO +CO![]() Cu +CO2;如固体只有氧化亚铜,验证方案为:取少年红色粉末,放于试管中,向其中加入足量稀硫酸,充分反应后溶液变为蓝色,仍有红色固体。则证明固体为氧化亚铜。一氧化碳和氧化铜的反应方程式为:2CuO +CO
Cu +CO2;如固体只有氧化亚铜,验证方案为:取少年红色粉末,放于试管中,向其中加入足量稀硫酸,充分反应后溶液变为蓝色,仍有红色固体。则证明固体为氧化亚铜。一氧化碳和氧化铜的反应方程式为:2CuO +CO![]() Cu2O +CO2;(2) 可作为计算依据的是:A.由反应前CuO粉末的质量可计算出如果生成铜或氧化亚铜时固体的质量,与实验所得固体质量对照即得结论;B.硬质玻璃管中固体物质减少的质量为氧化铜中氧元素的质量,如果减少的量等于氧元素的质量,则固体是由铜。如固体减少的质量小于氧化铜中氧元素的质量,则所得固体为氧化亚铜;C中一氧化碳是先通后停的,所以是过量的,因此其提供的质量无法用于计算;D.反应后固体混合物的总质量与氧化铜中铜元素的质量比较,可知剩余固体是铜还是氧化亚铜。
Cu2O +CO2;(2) 可作为计算依据的是:A.由反应前CuO粉末的质量可计算出如果生成铜或氧化亚铜时固体的质量,与实验所得固体质量对照即得结论;B.硬质玻璃管中固体物质减少的质量为氧化铜中氧元素的质量,如果减少的量等于氧元素的质量,则固体是由铜。如固体减少的质量小于氧化铜中氧元素的质量,则所得固体为氧化亚铜;C中一氧化碳是先通后停的,所以是过量的,因此其提供的质量无法用于计算;D.反应后固体混合物的总质量与氧化铜中铜元素的质量比较,可知剩余固体是铜还是氧化亚铜。

 名校课堂系列答案
名校课堂系列答案