题目内容
(8分)回收废旧干电池、保护环境是我们每个公民的义务,下面是我校化学兴趣小组探究回收废旧干电池意义的过程(片断),请帮助他们完成相应报告:
[提出问题] 废旧干电池的组成物质有什么?
[查阅资料] 1. 淀粉遇I2变蓝色 2. 部分酸碱盐溶解性表
[活动探究] 电池的内容物中有没有我们熟悉的离子?
[猜想1] 小组中某同学在剥开电池外壳时,闻到一股淡淡的刺激性气味,因此他猜想:电池的内容物中含有NH4+
[设计方案1] 取少量白色糊状物与 混合、研磨,闻到氨味,证明上述猜想正确。
[猜想2] 可能含有OH-、CO32-、Cl-、SO42-中的一种或几种。
[设计方案2]为了验证猜想2,设计如下实验,请完成表格中相应内容。
[结论]上述实验证明,电池内白色糊状物主要是 (一种盐化学式)和淀粉等两种物质混合而成。
[交流与讨论] 根据上述探究过程,你认为电池内容物有无回收价值?请简要说明理由 。
[提出问题] 废旧干电池的组成物质有什么?
[查阅资料] 1. 淀粉遇I2变蓝色 2. 部分酸碱盐溶解性表
 | OH- | NO3- | Cl- | SO42- | CO32- |
| H+ |  | 溶、挥 | 溶、挥 | 溶 | 溶、挥 |
| Ag+ |  | 溶 | 不溶 | 微溶 | 不溶 |
| Ba2+ | 溶 | 溶 | 溶 | 不 溶 | 不 溶 |
[猜想1] 小组中某同学在剥开电池外壳时,闻到一股淡淡的刺激性气味,因此他猜想:电池的内容物中含有NH4+
[设计方案1] 取少量白色糊状物与 混合、研磨,闻到氨味,证明上述猜想正确。
[猜想2] 可能含有OH-、CO32-、Cl-、SO42-中的一种或几种。
[设计方案2]为了验证猜想2,设计如下实验,请完成表格中相应内容。
| 操作步骤 | 实验现象 | 相应的结论 |
| 1.取样。溶于适量的水,静置,过滤。取少量滤液,滴加紫色石蕊试液。 | 石蕊试液不变蓝色 | 没有 存在 |
| 2.另取少量滤液,滴加过量的稀硝酸。 | 无明显现象 | 没有 存在 |
| 3.向第2步所得溶液中滴加少量的硝酸钡溶液 | | 没有SO42-存在 |
| 4.向第3步所得溶液中滴加少量硝酸银溶液 | 有白色沉淀产生 | 有 存在 |
| 5.取白色糊状物,滴加少量碘液 | | 则说明有淀粉存在 |
[交流与讨论] 根据上述探究过程,你认为电池内容物有无回收价值?请简要说明理由 。
[设计方案1] 熟石灰
[设计方案2]无OH- CO32- 无明显现象 Cl- 有蓝色出现
[结论] NH4Cl
[交流与讨论]有 因含有铵盐可做化肥(或答无,因物质量太少。合理答案即可。)
[设计方案2]无OH- CO32- 无明显现象 Cl- 有蓝色出现
[结论] NH4Cl
[交流与讨论]有 因含有铵盐可做化肥(或答无,因物质量太少。合理答案即可。)
试题分析:[设计方案1] 根据铵根离子的检验方法分析可知,可取少量白色糊状物与熟石灰混合研磨,看是否有刺激性气味的气体生成,如果能闻到氨味,证明上述猜想正确。
[设计方案2] 1、石蕊试液只有遇到碱性溶液才会变蓝,没有变蓝说明溶液不呈碱性,即没有氢氧根离子;
2、由于碳酸盐能与稀硝酸反应生成二氧化碳气体,故往溶液中滴加稀硝酸没有明显现象,说明溶液中无碳酸根离子;
3、根据硫酸根离子能与钡离子结合生成不溶于酸的白色沉淀,由于溶液中无硫酸根离子存在,故往溶液中加入硝酸钡后没有明显现象;
4、由于氯离子能与银离子结合生成不溶于稀硝酸的白色沉淀,故往溶液中滴加硝酸银有白色沉淀产生,说明溶液中含有氯离子;
5、由于碘具有遇淀粉变蓝的特性,所以当有淀粉存在时,滴加少量碘液会变蓝色。
[结论] 由以上实验不难得出白色糊状物中一定含有铵根离子和氯离子,故为NH4Cl。
[交流与讨论] 由于电池内容物中含有氯化铵,而氯化铵是一种氮肥,所以可以进行回收利用。
点评:本题考查了氢氧根离子、碳酸根离子、硫酸根离子、氯离子以及淀粉的检验,熟记这些离子的检验方法,以及反应的实验现象,是解题的关键。

练习册系列答案
相关题目
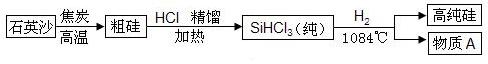
 Si +2CO↑,反应的类型是 反应(填“分解”“化合”“置换”“复分解”之一)。
Si +2CO↑,反应的类型是 反应(填“分解”“化合”“置换”“复分解”之一)。