题目内容
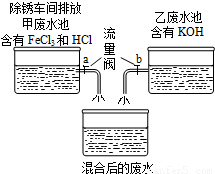
 课外小组的同学在参观废水处里厂时,得知除锈车间排放到甲废水池中含有的FeCl3、HCl与乙废水池中含有的KOH废水进行混合(如图).课外小组的同学对混合后的废水中溶质的成分进行了探究.
课外小组的同学在参观废水处里厂时,得知除锈车间排放到甲废水池中含有的FeCl3、HCl与乙废水池中含有的KOH废水进行混合(如图).课外小组的同学对混合后的废水中溶质的成分进行了探究.
(1)取适量废水,静置,取上层清液观察,发现废水呈黄色,说明废水中一定有________;
(2)向上述上层清液中滴加1~2滴紫色石蕊试液,发现紫色石蕊试液变红,说明废水中一定有________;
(3)同学们讨论后认为甲、乙废水混合后只发生了一个反应,请你写出该反应的化学方程式:________;
(4)为了使混合后的废水能浇灌农田,你应加大________(填“a”或“b”)阀的流量,并测定混合液的pH=7.
解:(1)废水呈黄色,说明废水中一定有氯化铁;
(2)紫色石蕊试液变红,说明废水呈酸性,所以废水中一定有盐酸;
(3)盐酸有剩余,所以氯化铁没有反应,只有盐酸和氢氧化钾反应生成氯化钾和水,反应的化学方程式:HCl+KOH=KCl+H2O;
(4)盐酸有剩余说明氢氧化钾少,所以应该加大乙废水池的流量.
故答案为:(1)FeCl3;(2)HCl;(3)HCl+KOH=KCl+H2O;(4)b.
分析:(1)根据废水呈黄色说明有氯化铁进行解答;
(2)根据紫色石蕊试液变红,说明废水呈酸性进行解答;
(3)根据盐酸和氢氧化钾反应生成氯化钾和水进行解答;
(4)根据盐酸有剩余说明氢氧化钾少,所以应该加大乙废水池的流量进行解答.
点评:根据酸、碱、盐之间能否发生反应和物质的溶解性判断物质的在水中的存在状况,并结合题中三种物质的限定对甲、乙两车间废水中的物质进行判断.
(2)紫色石蕊试液变红,说明废水呈酸性,所以废水中一定有盐酸;
(3)盐酸有剩余,所以氯化铁没有反应,只有盐酸和氢氧化钾反应生成氯化钾和水,反应的化学方程式:HCl+KOH=KCl+H2O;
(4)盐酸有剩余说明氢氧化钾少,所以应该加大乙废水池的流量.
故答案为:(1)FeCl3;(2)HCl;(3)HCl+KOH=KCl+H2O;(4)b.
分析:(1)根据废水呈黄色说明有氯化铁进行解答;
(2)根据紫色石蕊试液变红,说明废水呈酸性进行解答;
(3)根据盐酸和氢氧化钾反应生成氯化钾和水进行解答;
(4)根据盐酸有剩余说明氢氧化钾少,所以应该加大乙废水池的流量进行解答.
点评:根据酸、碱、盐之间能否发生反应和物质的溶解性判断物质的在水中的存在状况,并结合题中三种物质的限定对甲、乙两车间废水中的物质进行判断.

练习册系列答案
相关题目
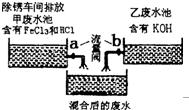 24、课外小组的同学在参观废水处里厂时,得知除锈车间排放到甲废水池中含有的FeCl3、HCl与乙废水池中含有的KOH废水进行混合(如图),课外小组的同学对混合后的废水池中的溶液进行探究.
24、课外小组的同学在参观废水处里厂时,得知除锈车间排放到甲废水池中含有的FeCl3、HCl与乙废水池中含有的KOH废水进行混合(如图),课外小组的同学对混合后的废水池中的溶液进行探究.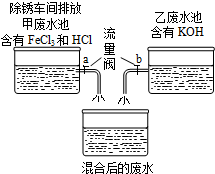 (2012?丹阳市二模)课外小组的同学在参观废水处里厂时,得知除锈车间排放到甲废水池中含有的FeCl3、HCl与乙废水池中含有的KOH废水进行混合(如图).课外小组的同学对混合后的废水中溶质的成分进行了探究.
(2012?丹阳市二模)课外小组的同学在参观废水处里厂时,得知除锈车间排放到甲废水池中含有的FeCl3、HCl与乙废水池中含有的KOH废水进行混合(如图).课外小组的同学对混合后的废水中溶质的成分进行了探究.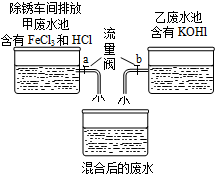 课外小组的同学在参观废水处里厂时,得知除锈车间排放到甲废水池中含有的FeCl3、HCl与乙废水池中含有的KOH废水进行混合(如图),课外小组的同学对混合后的废水池中的溶液进行探究.
课外小组的同学在参观废水处里厂时,得知除锈车间排放到甲废水池中含有的FeCl3、HCl与乙废水池中含有的KOH废水进行混合(如图),课外小组的同学对混合后的废水池中的溶液进行探究.