题目内容
【题目】化学是以实验为基础的科学,实验是科学探究的重要手段。
(1)某化学兴趣小组的同学利用图1微型实验装置进行探究实验。①挤压滴管后,写出单球管中发生反应的化学方程式_____。
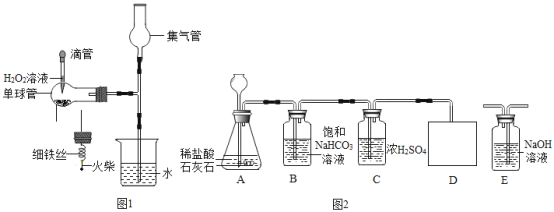
②点燃系在细铁丝下的火柴,待火柴快燃烧尽时立即插入充满氧气的集气管中并塞紧,观察到的实验现象是_____。
③采用微型实验装置的优点有哪些?(答出一条即可)_____
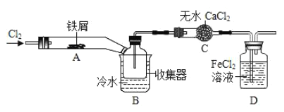
(2)另一化学兴趣小组选用图2装置制取纯净、干燥的CO2,并验证其部分性质。
①B装置中发生反应的化学方程式为_____。
②C装置中浓硫酸的作用是_____。
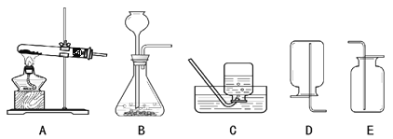
③请在D中简要补画出CO2的收集装置图_____。
④要证明在E装置中CO2与NaOH溶液发生了反应,应如何操作?(写出实验步骤和现象)_____
(3)将30g氯酸钾(KClO3)和二氧化锰的固体混合物装入试管中,加热制取氧气,同时生成氯化钾。待反应完全后,将试管冷却,称量,可以得到20.4g固体物质。请计算原固体混合物中氯酸钾的质量____。
【答案】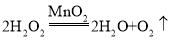 铁丝燃烧,火星四射,生成黑色固体,放出大量的热,集气管下端有气泡冒出 装置小,节约药品等 NaHCO3+HCl═NaCl+H2O+CO2↑ 干燥,除去二氧化碳中的水蒸气
铁丝燃烧,火星四射,生成黑色固体,放出大量的热,集气管下端有气泡冒出 装置小,节约药品等 NaHCO3+HCl═NaCl+H2O+CO2↑ 干燥,除去二氧化碳中的水蒸气 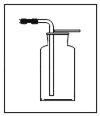 取少量反应后的液体,滴加足量的稀盐酸,看到有气泡产生;或者取少量反应后的液体,滴加氯化钙溶液,看到溶液变浑浊 24.5g
取少量反应后的液体,滴加足量的稀盐酸,看到有气泡产生;或者取少量反应后的液体,滴加氯化钙溶液,看到溶液变浑浊 24.5g
【解析】
(1)①挤压后,过氧化氢溶液和二氧化锰接触,所以单球管中发生反应是过氧化氢在二氧化锰的催化下生成水和氧气,对应的化学方程式是: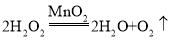 ;
;
②制取的气体收集在集气管中,点燃系在细铁丝下的火柴,待火柴快燃烧尽时立即插入充满氧气的集气管中并塞紧,由于铁丝在氧气中燃烧且放热,所以观察到的现象是铁丝燃烧,火星四射,生成黑色固体,放出大量的热,集气管下端有气泡冒出。
③采用微型实验装置的优点有装置小,节约药品等;
(2)①B装置中,碳酸氢钠和稀盐酸中挥发出的氯化氢反应生成氯化钠、水和二氧化碳,发生反应的化学方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑;
②浓硫酸具有吸性,C装置中浓硫酸的作用是吸收水蒸气;
③二氧化碳密度比空气大,可以用向上排空气法收集,如图所示: 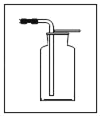 ;
;
④要证明在E装置中CO2与NaOH溶液发生了反应,实际就是检验碳酸根离子的存在,可以用沉淀法或者气化法,具体操作为:取少量反应后的液体,滴加足量的稀盐酸,看到有气泡产生;或者取少量反应后的液体,滴加氯化钙溶液,看到溶液变浑浊。
(3)根据质量守恒定律可知,生成氧气的质量为:30g﹣20.4g=9.6g;
设:原固体混合物中氯酸钾的质量为x。
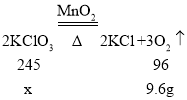
![]() x=24.5g。
x=24.5g。

 一课一练课时达标系列答案
一课一练课时达标系列答案