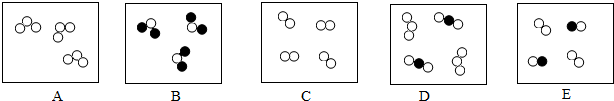
题目内容
将宏观、微观及化学符号联系在一起是化学学科的特点.
(1)A、B、C、D表示四种物质,其微观示意图如图1所示:
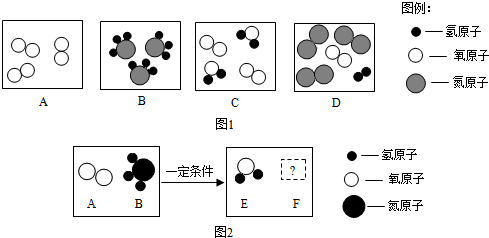
①从微观角度看,B中每个分子由 个原子构成.
②从宏观角度看,图中表示混合物的是 (填字母序号,下同),表示单质的是 .
(2)在一定条件下,A和B能发生化学反应生成E和F,其微观示意图如图2所示:
①若F为空气中体积分数最大的气体,则该反应中生成的B和F的质量比 .
②若F为氧化物,且A和B的分子个数比为5:4,则该反应的化学方程式为 .
(3)甲物质是一种重要的有机化工原料.一定质量的甲和48g氧气充分反应,当氧气完全反应时,可生成44g二氧化碳和36g水,则甲中所含各元素的质量比为
(4)服用碘片治疗I-131辐射的推荐服用剂量是每日摄入KI为130-170mg,假设服用某碘片每日补充166mgKI.已知每千克某品牌碘盐中KIO3的加入量为42.8mg,如果用该食盐替代碘片提供治疗辐射所需的碘元素,则每日需食用该食盐的质量为 kg.
(1)A、B、C、D表示四种物质,其微观示意图如图1所示:

①从微观角度看,B中每个分子由
②从宏观角度看,图中表示混合物的是
(2)在一定条件下,A和B能发生化学反应生成E和F,其微观示意图如图2所示:
①若F为空气中体积分数最大的气体,则该反应中生成的B和F的质量比
②若F为氧化物,且A和B的分子个数比为5:4,则该反应的化学方程式为
(3)甲物质是一种重要的有机化工原料.一定质量的甲和48g氧气充分反应,当氧气完全反应时,可生成44g二氧化碳和36g水,则甲中所含各元素的质量比为
(4)服用碘片治疗I-131辐射的推荐服用剂量是每日摄入KI为130-170mg,假设服用某碘片每日补充166mgKI.已知每千克某品牌碘盐中KIO3的加入量为42.8mg,如果用该食盐替代碘片提供治疗辐射所需的碘元素,则每日需食用该食盐的质量为
考点:微粒观点及模型图的应用,纯净物和混合物的判别,单质和化合物的判别,化合物中某元素的质量计算,书写化学方程式、文字表达式、电离方程式
专题:化学反应模拟图型
分析:(1)根据物质的微观构成,分析物质微粒的构成及物质的类别;
(2)
①F是空气中体积分数最大的气体-氮气时其反应物是氧气与氨气,产物是水与氮气,可书写出化学反应方程式,并对生成物的质量关系进行计算;
②依据质量守恒定律可知F一定是氮的氧化物,用AB的分子个数比可确定其化学式,进而写出方程式;
(3)根据质量守恒定律,则可求甲参加反应的质量,从而求甲中所含各元素的质量比;
(4)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,计算出166mgKI中含有碘元素的质量;由已知每千克某品牌碘盐中KIO3的加入量为42.8mg,计算出含有碘元素的质量,进而根据题意计算每日需食用该食盐的质量.
(2)
①F是空气中体积分数最大的气体-氮气时其反应物是氧气与氨气,产物是水与氮气,可书写出化学反应方程式,并对生成物的质量关系进行计算;
②依据质量守恒定律可知F一定是氮的氧化物,用AB的分子个数比可确定其化学式,进而写出方程式;
(3)根据质量守恒定律,则可求甲参加反应的质量,从而求甲中所含各元素的质量比;
(4)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,计算出166mgKI中含有碘元素的质量;由已知每千克某品牌碘盐中KIO3的加入量为42.8mg,计算出含有碘元素的质量,进而根据题意计算每日需食用该食盐的质量.
解答:解:
(1)
①由B分子的构成可知,B中每个分子由4个原子构成.
②由A、B、C、D表示四种物质的微观示意图可知,在C、D中都是由不同种分子构成的物质,从宏观上是由不同种物质组成的,属于混合物;在A中,是由同种原子构成的双原子分子构成的,宏观上是由同种元素组成的纯净物,属于单质;
(2)
①F是氮气时其反应物是氧气与氨气,产物是水与氮气,其方程式是3O2+4NH3
6H2O+2N2,则水与氮气的质量比=(6×18):(4×14)=27:14;
②依据质量守恒定律可知F一定是氮的氧化物,因AB的分子个数比5:4,进而写出方程式是5O2+4NH3
6H2O+4NO;
(3)根据质量守恒定律,则可求甲参加反应的质量为:44+36-48=32克;二氧化碳中的碳元素的质量为44克×
×100%=12克,水中氢元素的质量为36克×
×100%=4克;因为碳元素、氢元素都来自甲,故甲中各元素的质量比m(C):m(H)=12:4;生成物中的氧元素的质量是44+36-12-4=64g,而反应物中氧气提供的氧元素的质量是48g,所以甲中含有的氧元素的16g,所以碳氢氧的质量比是3:1:4;
(4)166mgKI中含有碘元素的质量为:166mg×
×100%=127mg;
已知每千克某品牌碘盐中KIO3的加入量为42.8mg,含碘元素的质量为:42.8mg×
×100%=25.4mg;
如果用该食盐替代碘片提供治疗辐射所需的碘元素,则每日需食用该食盐的质量为
×1Kg=5Kg
答案:
(1)①4 ②CD A
(2)①27:14;②5O2+4NH3
6H2O+4NO
(3)3:1:4
(4)5
(1)
①由B分子的构成可知,B中每个分子由4个原子构成.
②由A、B、C、D表示四种物质的微观示意图可知,在C、D中都是由不同种分子构成的物质,从宏观上是由不同种物质组成的,属于混合物;在A中,是由同种原子构成的双原子分子构成的,宏观上是由同种元素组成的纯净物,属于单质;
(2)
①F是氮气时其反应物是氧气与氨气,产物是水与氮气,其方程式是3O2+4NH3
| ||
②依据质量守恒定律可知F一定是氮的氧化物,因AB的分子个数比5:4,进而写出方程式是5O2+4NH3
| ||
(3)根据质量守恒定律,则可求甲参加反应的质量为:44+36-48=32克;二氧化碳中的碳元素的质量为44克×
| 12 |
| 44 |
| 2 |
| 18 |
(4)166mgKI中含有碘元素的质量为:166mg×
| 127 |
| 39+127 |
已知每千克某品牌碘盐中KIO3的加入量为42.8mg,含碘元素的质量为:42.8mg×
| 127 |
| 39+127+16×3 |
如果用该食盐替代碘片提供治疗辐射所需的碘元素,则每日需食用该食盐的质量为
| 127mg |
| 25.4mg |
答案:
(1)①4 ②CD A
(2)①27:14;②5O2+4NH3
| ||
(3)3:1:4
(4)5
点评:本题以反应示意图为载体,考查化学方程式的书写及计算,分子由原子构成,同种原子构成的分子为单质分子,不同种原子构成的分子为化合物分子并书写出化学式连接成化学方程式.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 甲型H1N1流感病毒正威胁着人类的健康和安全.“达菲”(C16H28O4N2)是目前世界上治疗H1N1流感病毒的良药.生产“达菲”的主要原料是莽草酸,可从茴香中提取.回答下列问题:
甲型H1N1流感病毒正威胁着人类的健康和安全.“达菲”(C16H28O4N2)是目前世界上治疗H1N1流感病毒的良药.生产“达菲”的主要原料是莽草酸,可从茴香中提取.回答下列问题: 某化学兴趣小组同学设计了如图所示的实验装置,既可用于制取气体,又可用于探究物质性质.
某化学兴趣小组同学设计了如图所示的实验装置,既可用于制取气体,又可用于探究物质性质.