题目内容
【题目】我们学习了氧气和二氧化碳的制法,并到实验室体验了化学实验的奇妙与乐趣,请回答问题.
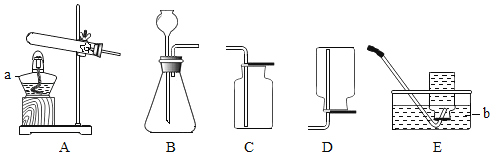
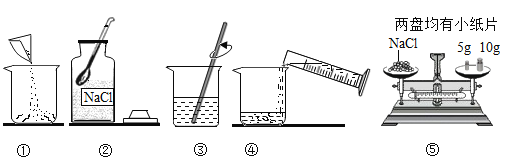
(1)写出如图装置中标号仪器的名称:a_____;b_____.
(2)若用高锰酸钾制取氧气,则反应的化学方程式_____,该反应属于的基本反应类型为:_____.
(3)实验室用大理石与稀盐酸反应制取二氧化碳,发生的化学反应的化学方程式为_____,应选用的发生装置是_____,收集装置是_____,要验证二氧化碳是否收集满的方法是_____.
(4)实验室用锌与稀硫酸反应制取氢气,应选用的发生装置为_____,请写出反应的化学方程式_____.
【答案】酒精灯 水槽 2KMnO4![]() K2MnO4+MnO2+O2↑ 分解反应 CaCO3+2HCl=CaCl2+H2O+CO2↑ B C 一根燃着的木条平放在集气瓶口,木条熄灭,证明满了 B Zn+H2SO4=ZnSO4+H2↑
K2MnO4+MnO2+O2↑ 分解反应 CaCO3+2HCl=CaCl2+H2O+CO2↑ B C 一根燃着的木条平放在集气瓶口,木条熄灭,证明满了 B Zn+H2SO4=ZnSO4+H2↑
【解析】
(1)给物质加热的仪器是酒精灯,盛水的容器是水槽,故填:酒精灯、水槽;
(2)高锰酸钾受热分解成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4![]() K2MnO4+MnO2+O2↑,符合“一变多”的特征,属于分解反应;
K2MnO4+MnO2+O2↑,符合“一变多”的特征,属于分解反应;
(3)实验室制取二氧化碳,是在常温下,用大理石或石灰石和稀盐酸制取的,石灰石的主要成分是碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,化学方程式: CaCO3+2HCl=CaCl2+H2O+CO2↑;大理石和石灰石是固体,稀盐酸是液体,反应条件是常温,选择固液常温型装置,故选装置B;CO2密度比空气大,能溶于水,采用向上排空气法,故选装置C;
(4)实验室制取氢气,是在常温下用锌和稀硫酸反应,锌是固体,稀硫酸是液体,因此选择固液常温型装置,故选装置B;锌与稀硫酸反应生成硫酸锌与氢气,化学方程式为:Zn+H2SO4=ZnSO4+H2↑。