题目内容
【题目】下图是部分元素周期表和砷元素(As)的信息,据此回答下列问题:
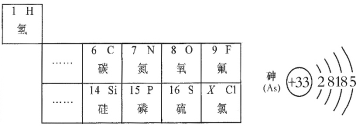
(1)空气中含量最多的元素的原子序数是_________。
(2)画出原子序数为X的原子的结构示意图 _________,化学反应中该原子容易_______(填“得到”或“失去”)电子。
(3)砷(As)元素位于元素周期表第___周期,____主族,砷元素与表中磷元素的化学性质________,(填“相似”或“不相似”)。
(4)查阅资料:具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质。下列各组粒子中属于等电子体是_____(填字母序号)
A. NO和O2 B. CH4和NH4+ C. H2O和CO2 D. PO43ˉ和CO32ˉ
【答案】7 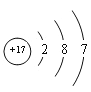 失去 四 ⅤA 相似 BD
失去 四 ⅤA 相似 BD
【解析】
(1)空气中含量最多的元素是氮,由元素周期表可知,原子序数为7;
(2)元素周期表中原子序数依次增加,所以X为17,原子的结构示意图为: ;最外层电子数为7,在化学反应中容易失去电子;
;最外层电子数为7,在化学反应中容易失去电子;
(3)根据砷(As)元素原子的电子排布是四个电子层,最外层电子数为5,故处于第四周期第ⅤA族;砷元素与磷元素的最外层电子数相等,故化学性质相似;
(4)等电子体在计算时,是将组成的各原子的电子数相加所得的和,磷酸根和硫酸根的原子个数和电子个数都相等,属于等电子体;NO和O2的原子数相同,但是电子数不相同;CH4和NH4+的原子数相同,电子数相同; H2O和CO2的原子数相同,但是电子数不相同;PO43ˉ和CO32ˉ的原子数相同,电子数相同。

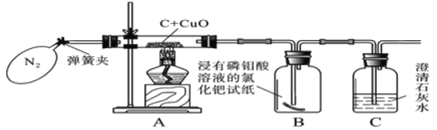
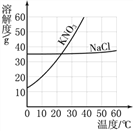
【题目】如下表中数据为氯化钠和硝酸钾在不同温度时的溶解度,如图所示是用其中一种物质所做的实验。下列分析正确的是( )

温度(℃) | 10 | 20 | 30 | 40 | |
溶解度/g | KNO3 | 20.9 | 31.6 | 45.8 | 63.9 |
NaCl | 35.8 | 36.0 | 36.3 | 36.6 | |
A. 实验中加入的物质R是氯化钠 B. ④中t的取值范围在30~40之间
C. ③中的溶液可能是饱和溶液 D. ④中溶液的溶质质量分数可能比②中的大