��Ŀ����
��18�֣������������ճ������г��õĸ�����ϴ����ѡ���ʵ�����Ʒ���Եõ����õ���ϴЧ����
|
���� |
ϴ�ྫ |
����� |
¯������ |
���ձ�ը�� |
Ư�� |
|
��Ʒ��ʽ |
|
|
|
|
|
|
��Ч�ɷ� ���� |
��ϴ���� |
���� |
�������� |
��̼���� |
���� |
��1��ʹ��ϴ�ྫ��ϴ�;��ϵ����ۣ�������Ϊ������ �Ĺ��ܡ�
��2���������ʿ���ʹ�ý������ϴ���� ������ĸ��ţ���
a������ b������ c��ˮ������Ҫ�ɷ�Ϊ̼��ƺ�������þ��[��Դ:Z#xx#k.Com]
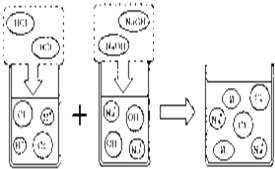
��3��ȡ����һ������¯���������μӼ��η�̪��Һ����Һ�� ɫ�������������¯��������ϣ����Է�����ͼ��ʾ�Ļ�ѧ��Ӧ��ͼ��a��������Ϊ ��

��4�������ձ�ը�Ρ�����ˮ�������Na2CO3��H2O2������ը������ˮ���ټ��������Ľ���飬�����Ļ�ѧ��Ӧ����ʽΪ ��
��5����ѧС�鷢��һ����װ�����Ư�ۣ�ͬѧ�Ƕ�Ư����Ư�������Ƿ�ʧЧ���������ʡ�������Ч�ɷ���ȫ��ʧʱ����Ư�۾���ȫʧЧ��������ʧʱ����Ϊ����ʧЧ����
���������ϡ�
��Ư�۵���Ҫ�ɷ���Ca(ClO)2��CaCl2��Ca(OH)2������Ч�ɷ���Ca(ClO)2��
��Ca(ClO)2������ˮ��Ư��ԭ���ǣ����ڿ����з�����Ӧ�� Ca(ClO)2+H2O+CO2=CaCO3��+2HClO��

�� HClO���ȶ����ֽ�����HCl��һ�ֳ����ĵ������塣
�� CaCl2��ˮ��Һ�����ԣ�HClO��ˮ��Һ�����ԡ�
�� HClO�ܿ�ʹ��ɫ���ʣ��磺Ʒ����Һ����ɫ��
��ʵ��̽�����±���̽��ijƯ���Ƿ���ȫʧЧ��ʵ�飬����ݱ��н��ۣ�������ա�
|
ʵ�鲽�� |
ʵ������ |
ʵ����� |
|
������Ư����Ʒ����ˮ�У�ͨ��������CO2���壬 �� |
|
Ư�۵�Ư����������ȫʧЧ |
������̽����ͬѧ�Ƕ�ij��ȫʧЧ���Ư�۵ijɷֺܸ���Ȥ��������һ��̽��������ʦ�İ����£�ͬѧ�ǶԸ�ʧЧ���Ư�۳ɷֽ��в��룺
����һ��CaCl2��CaCO3��������� ��Ȼ�����ʵ��̽����
|
ʵ����� |
ʵ������ |
ʵ����� |
|
����Ʒ����ˮ�У�����ܽ����ˣ�_______________�� |
______________ |
����һ���� |
���������ۡ�
��HClO�ֽ�ʱ������HCl�⣬���ɵ���һ�ֳ��������� ��
�ڲ����еijɷ�CaCO3����Ư�۵���Ч�ɷ��ڿ����з�����Ӧ�����⣬����������Դ�������û�ѧ����ʽ��ʾ ��
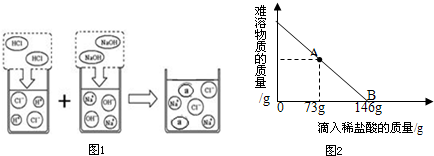
�������о���ȡ����Ư��31.1g��һ�ձ��У������м���131.7gˮ��ʹƯ���еĿ�������ȫ�ܽ⡣Ȼ������������μ���������������Ϊ10%��ϡ���ᣬ�ձ������ܹ������ʵ�������������ϡ�����������ϵ������ͼ��ʾ�����������ش��������⣺
�ٵ�����10%��ϡ������ͼ��A��ʱ���ձ�����Һ�ﺬ�е������ǣ�д��ѧʽ��________��
�ڵ�����10%��ϡ����146gʱ����B�㣩����ͨ�����㣬���ʱ�ձ������ò�������Һ�����ʵ�����������

��1���黯 ��2��a c ��3���죻ˮ���ӣ�4��Na2CO3+2HCl = 2NaCl+H2O+CO2����2�֣���5��
��ʵ��̽��������Ʒ����Һ��Ʒ����Һ����ɫ
������̽�����������CaCl2��CaCO3��Ca(OH)2��ȡ��Һ���Թ��У������е�����ɫ��̪��Һ��ͨ��CO2����Һ�����Ա仯��
���������ۡ�����������O2�� ��Ca(OH)2+CO2=CaCO3��+H2O��2�֣�
���������
��CaCl2��11.1% �������Һ��CaCl2������Ϊ22.2g+31.1g-20g=33.3g 1�������Һ������Ϊ146g+31. 1g+131.7g-8.8g=300g 1�����������������Ϊ11.1% 1�֣�
����������1��ϴ����ϴ�Ӳ;��ϵ�������Ҫ������ϴ�Ӽ����Խ����ۺ�ˮ����һ�����ȥ���������ó����黯���ã�
��2�������ijɷ������ᣬ���Ժ����ⷴӦ��������ˮ���ʳ�ȥ�����Ժ�ˮ����Ӧ����������ˮ�����ʳ�ȥ�������ܺ����۷�Ӧ��
��3��¯����������Ҫ�ɷ����Լ��Ե��������ƣ����ԵμӼ��η�̪��Һ����Һ���ɫ��������������Ʒ�Ӧ���������ӷ�Ӧԭ��֪�������Ȼ����������Ӻ���������ʽ���ڣ�ˮ��Ҫ��ˮ������ʽ���ڣ�����죻H2O��ˮ���ӣ�
��4��������ѧ֪ʶ֪��̼���ƺ����ᷴӦ�����Ȼ��ơ�������̼���壬�仯ѧ��Ӧ����ʽΪ��Na2CO3+2HCl=2NaCl+H2O+CO2����
��ʵ��̽����������Ca��ClO��2+H2O+CO2=CaCO3+2HClO��HClO��ʹ��ɫ������Ʒ����Һ��ɫ�����Կ�������Ʒ����ɫ��ȥ���ʵ�飮����Ʒ����Һ�������ɫ����ȥ��˵��Ư��ʧЧ���ʴ�Ϊ������Ʒ����Һ��Ʒ����Һ����ɫ
�������������Ŀ��Ϣ��֪��Ư�۵���Ҫ�ɷ���Ca��ClO��2��CaCl2��Ca��OH��2��Ca��ClO��2+H2O+CO2=CaCO3+2HClO�����ǿ����ж�CaCl2��CaCO3��Ca��OH��2
�ʴ�Ϊ��CaCl2��CaCO3��Ca��OH��2��ȡ��Һ���Թ��У������е�����ɫ��̪��Һ��ͨ��CO2����Һ�����Ա仯
���������ۡ���HClO���ȶ����ֽ�����HCl��һ�ֳ�������ɫ��ζ���嶨�ɿ�֪����һ�����������ʴ�Ϊ��������O2����
�ڸ������ʵ���ɣ����ǿ��Զ϶��������ƺͶ�����̼����̼��ƣ�
�ʴ�Ϊ��Ca��OH��2+CO2=CaCO3��+H2O
�������о�����������̼��Ƶ�����Ϊa����Ӧ�����Ȼ��Ƶ�����Ϊb�����ɶ�����̼������Ϊc������ͼ��֪�μӷ�Ӧ���������Ϊ146g,�����Ȼ��������Ϊ 146g��10%=14.6g��
CaCO3 + 2HCl = CaCl2+H2O+CO2��
100 73 111 44
a 14.6g b c
100/73=a/14.6g 73/111=14.6g/b 73/44=14.6g/c
��ã�a=20g b=22.2g c=8.8g
����Һ�����ʵ�����Ϊ��22.2g+31.1g-20g=33.3g����Һ������Ϊ146g+31. 1g+131.7g-8.8g=300g������������Ϊ��33.3g/300g��100%=11.1%.


























 ��1������ʹ��ϴ������ϴ�;��ϵ����ۣ�������Ϊ������
��1������ʹ��ϴ������ϴ�;��ϵ����ۣ�������Ϊ������