题目内容
有A、B、C、D四种元素,A元素的原子只有一个质子,B元素是组成有机化合物不可缺少的元素,C元素是植物必需的一种营养元素,它能促进植物生长,增强抗倒伏的能力, D2-的电子层结构与氖原子相同。
(1)A元素组成单质的化学式为 ,(2)B元素的名称为 ,
(3)D的离子符号为 ,(4)A、C、D三种元素组成化合物的化学式为
(1)A元素组成单质的化学式为 ,(2)B元素的名称为 ,
(3)D的离子符号为 ,(4)A、C、D三种元素组成化合物的化学式为
⑴ H2 ⑵ 碳元素 ⑶ O2- ⑷ KOH
A元素中只有一个质子,可以知道A为氢元素,B元素是组成有机化合物不可缺少的元素,可以知道B为碳元素,C元素是植物必需的一种营养元素,它能促进植物生长,增强抗倒伏的能力,可知C为钾元素,D得到两个电子后与氖原子的结构相同可以知道D为氧元素,至此四种元素鉴定完毕,可以据此答题

练习册系列答案
相关题目

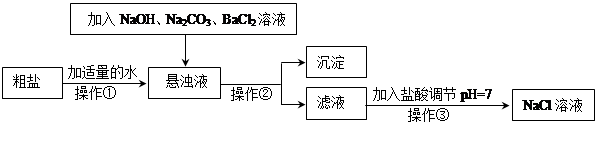 回答下列问题:
回答下列问题: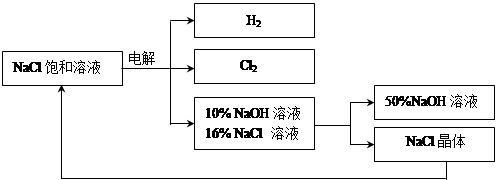
 Cl2 ↑+ H2 ↑ + 2NaOH,电解后溶液的pH 。(填“升高”、“不变”、“降低”)
Cl2 ↑+ H2 ↑ + 2NaOH,电解后溶液的pH 。(填“升高”、“不变”、“降低”)