题目内容
【题目】海水晒盐能够得到粗盐和卤水。卤水中含有MgCl2、KCl和MgSO4等物质,下图是它们的溶解度曲线。完成下列填空。
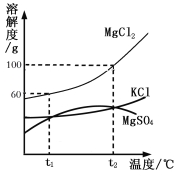
(1)在t1℃时,向100 g水中加入150 g MgCl2,形成 (填“饱和”或“不饱和”)溶液,将其温度升高到t2℃时,此时溶液中溶质的质量分数为 。
(2)t1℃时,MgCl2、KCl和MgSO4三种物质的饱和溶液中,溶质质量分数最大的是 。将t2℃时MgCl2、KCl和MgSO4三种物质的饱和溶液降温至t1℃时,可能会析出的晶体有 (填字母序号)。
A.MgCl2和KCl B.只有MgSO4 C.MgCl2、KCl和MgSO4
【答案】(1)饱和; 50%; (2)MgCl2 C
【解析】
试题分析:根据溶解度曲线可知(1)在t1℃时,氯化镁的溶解度为60g,故向100 g水中加入150 g MgCl2,形成饱和溶液,将其温度升高到t2℃时,溶解度为100g,故此时溶液中溶质的质量分数为100g/(100g+100g)×100%=50%;(2)根据饱和溶液的溶质的质量分数的表达式=溶解度/(100g+溶解度)×100%;可知溶解度大的物质,溶质的质量分数就大;故t1℃时,MgCl2、KCl和MgSO4三种物质的饱和溶液中,溶质质量分数最大的是氯化镁;将t2℃时MgCl2、KCl和MgSO4三种物质的饱和溶液降温至t1℃时,三种物质都会析出的晶体,因为三者的溶解度随温度的降低而减小。

练习册系列答案
相关题目