题目内容
下表列出了KNO3在不同温度下的溶解度.
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
(2)20℃时,把40g KNO3放入小烧杯中,然后再加100g水不断搅拌,形成溶液的质量为______g;该溶液是______(填“饱和”或“不饱和”)溶液.
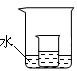
(3)如图所示,把上述(2)中的小烧杯放到盛水的大烧杯中.若将少量的下列物质分别小心地加入到大烧杯的水中,不断搅拌,能够使小烧杯中的KNO3溶液溶质的质量分数增大的是______(填序号).
①浓硫酸 ②硝酸铵 ③氢氧化钠 ④冰.
解:(1)从图中可以看出,硝酸钾的溶解度随温度的升高而增大.故答案为:溶解度随温度的升高而增大;
(2)20℃时,在100克水中,最多能溶解31.6克硝酸钾就能形成饱和溶液;所以40克硝酸钾放入100克水中,不能全部溶解.故答案为:131.6;饱和
(3)温度越高,硝酸钾的溶解度越大,饱和溶液的质量分数就越大.而浓硫酸、氢氧化钠固体溶于水能使溶液的温度升高.故答案为:①③
分析:(1)从硝酸钾在不同温度下的溶解度表可以看出,温度越高,溶解度越大;
(2)在20℃时,硝酸钾的溶解度是31.6克.即20℃时,在100克水中,最多能溶解31.6克硝酸钾就能形成饱和溶液;
(3)浓硫酸或氢氧化钠固体溶于水,溶液的温度升高.
点评:此题考查了多个知识点.从硝酸钾的溶解度表可以看出,温度越高,溶解度越大,饱和溶液的溶质的质量分数就越大.而氢氧化钠固体、浓硫酸溶于水会使溶液的温度升高.所以向溶液中加入氢氧化钠固体或浓硫酸,溶质的质量分数会增大.
(2)20℃时,在100克水中,最多能溶解31.6克硝酸钾就能形成饱和溶液;所以40克硝酸钾放入100克水中,不能全部溶解.故答案为:131.6;饱和
(3)温度越高,硝酸钾的溶解度越大,饱和溶液的质量分数就越大.而浓硫酸、氢氧化钠固体溶于水能使溶液的温度升高.故答案为:①③
分析:(1)从硝酸钾在不同温度下的溶解度表可以看出,温度越高,溶解度越大;
(2)在20℃时,硝酸钾的溶解度是31.6克.即20℃时,在100克水中,最多能溶解31.6克硝酸钾就能形成饱和溶液;
(3)浓硫酸或氢氧化钠固体溶于水,溶液的温度升高.
点评:此题考查了多个知识点.从硝酸钾的溶解度表可以看出,温度越高,溶解度越大,饱和溶液的溶质的质量分数就越大.而氢氧化钠固体、浓硫酸溶于水会使溶液的温度升高.所以向溶液中加入氢氧化钠固体或浓硫酸,溶质的质量分数会增大.

练习册系列答案
相关题目
20.(2009?梅州)下表列出了KNO3在不同温度下的溶解度.
(1)由上表可推出KNO3溶解度曲线的变化规律是KNO3溶解度随温度升高而.
(2)在20℃时,把40 g KNO3放入小烧杯中,然后再加入100 g水不断搅拌,形成溶液的质量为g;该溶液是(填“饱和”或“不饱和”)溶液.
(3)如图所示,把上述(2)中的小烧杯放到盛水的大烧杯中.若将少量的下列物质分别小心地加入到大烧杯的水中,不断搅拌,能够使小烧杯中的KNO3溶液溶质的质量分数增大的是(填序号).①浓硫酸,②硝酸铵,③氢氧化钠,④冰
(4)60℃时,把55g KNO3溶于水配成饱和溶液,最多可配得饱和溶液的质量为g.

| 温度/℃ | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
(2)在20℃时,把40 g KNO3放入小烧杯中,然后再加入100 g水不断搅拌,形成溶液的质量为g;该溶液是(填“饱和”或“不饱和”)溶液.
(3)如图所示,把上述(2)中的小烧杯放到盛水的大烧杯中.若将少量的下列物质分别小心地加入到大烧杯的水中,不断搅拌,能够使小烧杯中的KNO3溶液溶质的质量分数增大的是(填序号).①浓硫酸,②硝酸铵,③氢氧化钠,④冰
(4)60℃时,把55g KNO3溶于水配成饱和溶液,最多可配得饱和溶液的质量为g.

 19、下表列出了KNO3在不同温度下的溶解度.
19、下表列出了KNO3在不同温度下的溶解度.


 下表列出了KNO3在不同温度下的溶解度.
下表列出了KNO3在不同温度下的溶解度.