题目内容
依据下列实验所得到的结论准确的是
| 选项 | A | B | C | D |
| 实验设计 | 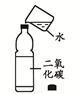 | 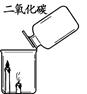 | 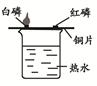 | 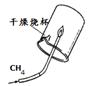 |
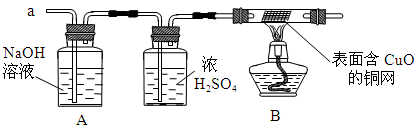
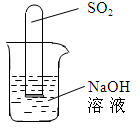
| 实验结论 | 二氧化碳与水反应生成碳酸 | 二氧化碳不支持燃烧、密度大于空气 | 可燃物燃烧温度需要达到着火点 | 既可说明甲烷具有可燃性,又说明了甲烷是由氢元素和碳元素组成 |
C
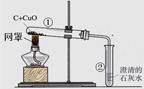
试题分析:二氧化碳能与水反应,也能溶于水,A实验不能证明二氧化碳与水反应生成了碳酸;二氧化碳不能燃烧,也不支持燃烧,密度大于空气,阶梯蜡烛从下到上依次熄灭;在相同温度下,白磷燃烧,红磷不燃烧,说明可燃物燃烧温度需要达到着火点;D图中甲烷燃烧实验,可以说明甲烷具有可燃性,甲烷中含有氢元素,不能证明其中含有碳元素。选C。
点评:二氧化碳不能燃烧,也不支持燃烧,密度大于空气,可做灭火剂;
燃烧必须同时具备三个条件才可以:1、有可燃物;2、可燃物与氧气接触;3、温度达到可燃物的着火点。

练习册系列答案
相关题目