题目内容
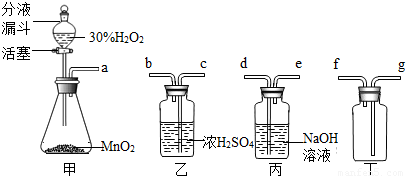
已知2H2O2 2H2O+O2↑实验室中利用该反应,选用下图所示装置课制取氧气.
2H2O+O2↑实验室中利用该反应,选用下图所示装置课制取氧气.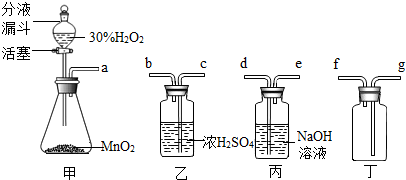
请回答下列问题:
(1)制取干燥氧气时,所选用装置导管接口顺序为(按字母)______,检查氧气气满的方法是:______.
(2)如将丁装置充满水,就可用排水法收集氧气,此时装置最合理的连接顺序为(按字母)______;
(3)若只改变装置中的药品,此装置还可以用来制取的气体是______.制取该气体的化学方程式为______.
解:(1)制取干燥氧气时,应将氧气通入到浓硫酸中,又由于氧气的密度大于空气的密度,所以,连接的顺序是:a-c-b-g;因为氧气能支持燃烧,所以验满的方法是:将带火星的木条放到导管口,若木条复燃,则氧气集满;
(2)因为氧气的密度小于水的密度,所以,如将丁装置充满水,此时装置最合理的连接顺序是a-f;
(3)根据装置可知,反应物的状态可以是固体和液体,反应条件是不需加热,此装置还可以用来制取二氧化碳气体,反应的方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑.
故答为:(1)a-c-b-g 将带火星的木条放到导管口,若木条复燃,则氧气集满;(2)a-f; (3)二氧化碳,CaCO3+2HCl=CaCl2+H2O+CO2↑.
分析:(1)根据制取干燥氧气时,应将气体通入到浓硫酸中,再结合氧气的密度分析装置连接的顺序,根据氧气的性质分析验满的方法;
(2)根据氧气和水的密度分析装置连接的顺序;
(3)根据装置分析制取气体的反应物状态和反应条件,选择药品,写出反应的方程式.
点评:本题主要考查了装置的选择与连接,要想解答好这类题目,就要熟记仪器装配或连接的方法、实验的基本原则和有关注意事项等等.
(2)因为氧气的密度小于水的密度,所以,如将丁装置充满水,此时装置最合理的连接顺序是a-f;
(3)根据装置可知,反应物的状态可以是固体和液体,反应条件是不需加热,此装置还可以用来制取二氧化碳气体,反应的方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑.
故答为:(1)a-c-b-g 将带火星的木条放到导管口,若木条复燃,则氧气集满;(2)a-f; (3)二氧化碳,CaCO3+2HCl=CaCl2+H2O+CO2↑.
分析:(1)根据制取干燥氧气时,应将气体通入到浓硫酸中,再结合氧气的密度分析装置连接的顺序,根据氧气的性质分析验满的方法;
(2)根据氧气和水的密度分析装置连接的顺序;
(3)根据装置分析制取气体的反应物状态和反应条件,选择药品,写出反应的方程式.
点评:本题主要考查了装置的选择与连接,要想解答好这类题目,就要熟记仪器装配或连接的方法、实验的基本原则和有关注意事项等等.

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目
已知2H2O2 2H2O+O2↑,CuSO4溶液对过氧化氢的分解也具有催化作用.有同学猜想其它盐溶液是否也能在这个反应中起同样的作用.于是他们做了以下的探究:
2H2O+O2↑,CuSO4溶液对过氧化氢的分解也具有催化作用.有同学猜想其它盐溶液是否也能在这个反应中起同样的作用.于是他们做了以下的探究:
(1)请你帮助他们完成实验报告:
| 实验过程 | 实验现象 | 实验结论 |
| 在一支试管中加5mL5%的H2O2溶液,然后滴入适量的FeCl3溶液,把带火星的木条伸入试管 | FeCl3溶液可以催化分解H2O2 |
甲同学的猜想是:真正催化分解H2O2的是FeCl3溶液中的Fe3+,
乙同学的猜想是:真正催化分解H2O2的是FeCl3溶液中的Cl-,
(3)同学们对甲、乙两位同学的猜想,用实验进行了探究.请你仔细分析后完成实验报告:
| 实验过程 | 实验现象 | 实验结论 |
| 向盛有5mL5%的H2O2溶液的试管中加入少量的稀盐酸,并把带火星的木条伸入试管 | 无明显现象 | |
| 向盛有5mL5%的H2O2溶液的试管中加入少量的 ,并把带火星的木条伸入试管 |
已知2H2O2![]() 2H2O+O2↑溶液对过氧化氢的分解也具有催化作用。有同学猜想其他盐溶液是否也能在这个反应中起同样的作用,于是他们做了以下的探究:
2H2O+O2↑溶液对过氧化氢的分解也具有催化作用。有同学猜想其他盐溶液是否也能在这个反应中起同样的作用,于是他们做了以下的探究:
(1)请你帮助他们完成实验报告:

(2)已知FeCl3在水中可电离出Fe3+和Cl-,同学们提出以下猜想:
甲同学的猜想是:真正催化分解H2O2的是FeCl3溶液中的Fe3+
乙同学的猜想是:真正催化分解H2O2的是FeCl3溶液中的Cl-
(3)同学们对甲、乙两位同学的猜想,用实验进行了探究。请你仔细分析后完成
实验报告:
| 实验过程 | 实验现象 | 实验结论 |
| 向盛有5 mL5%的H2O2溶液的试管中加入少量的稀盐酸,并把带火星的木条伸入试管 | 无明显现象 | |
| 向盛有5 mL 5%的H2O2溶液的试管中加入少量的_______,并把带火星的木条伸入试管 |
已知2H2O2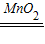 2H2O+O2↑,CuSO4溶液对过氧化氢的分解也具有催化作用.有同学猜想其它盐溶液是否也能在这个反应中起同样的作用.于是他们做了以下的探究:
2H2O+O2↑,CuSO4溶液对过氧化氢的分解也具有催化作用.有同学猜想其它盐溶液是否也能在这个反应中起同样的作用.于是他们做了以下的探究:
(1)请你帮助他们完成实验报告:
(2)已知FeCl3在水中可电离出Fe3+和Cl-,同学们提出以下设想:
甲同学的猜想是:真正催化分解H2O2的是FeCl3溶液中的Fe3+,
乙同学的猜想是:真正催化分解H2O2的是FeCl3溶液中的Cl-,
(3)同学们对甲、乙两位同学的猜想,用实验进行了探究.请你仔细分析后完成实验报告:
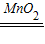 2H2O+O2↑,CuSO4溶液对过氧化氢的分解也具有催化作用.有同学猜想其它盐溶液是否也能在这个反应中起同样的作用.于是他们做了以下的探究:
2H2O+O2↑,CuSO4溶液对过氧化氢的分解也具有催化作用.有同学猜想其它盐溶液是否也能在这个反应中起同样的作用.于是他们做了以下的探究:(1)请你帮助他们完成实验报告:
| 实验过程 | 实验现象 | 实验结论 |
| 在一支试管中加5mL5%的H2O2溶液,然后滴入适量的FeCl3溶液,把带火星的木条伸入试管 | FeCl3溶液可以催化分解H2O2 |
甲同学的猜想是:真正催化分解H2O2的是FeCl3溶液中的Fe3+,
乙同学的猜想是:真正催化分解H2O2的是FeCl3溶液中的Cl-,
(3)同学们对甲、乙两位同学的猜想,用实验进行了探究.请你仔细分析后完成实验报告:
| 实验过程 | 实验现象 | 实验结论 |
| 向盛有5mL5%的H2O2溶液的试管中加入少量的稀盐酸,并把带火星的木条伸入试管______ | 无明显现象 | |
| 向盛有5mL5%的H2O2溶液的试管中加入少量的 ______,并把带火星的木条伸入试管 |
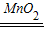 2H2O+O2↑实验室中利用该反应,选用下图所示装置课制取氧气.
2H2O+O2↑实验室中利用该反应,选用下图所示装置课制取氧气.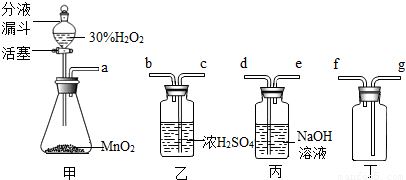
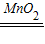 2H2O+O2↑,实验室中利用该反应,选用下图所示装置可制取氧气.
2H2O+O2↑,实验室中利用该反应,选用下图所示装置可制取氧气.